�ѻ�2D���������ܵ��о�
����֯��ѧԺ �˲���
��Ҫ
��2D�������ѻ��ǽ���2D����֯���ͷż�ȩ�����������ǿ�ȵ�һ�ֱȽ���Ч�ķ������������Ҵ����ѻ��������ò�ͬ�ĺϳɷ������õ����ֲ�ͬ�����ѻ�2D��֬������������֯���������е���ܡ������Ժ��ͷż�ȩֵ�����˷����Ƚϣ����������ƷFixapret COC�Ƚϡ�ʵ��֤����(1)���Ҵ����泣�õļ״���2D�����ѻ������Եõ��ͼ�ȩ������֬��(2)2D�����ǻ����ѻ��ܽ�������֯����ͷż�ȩ������ϵ��ǻ����ѻ����������ǿ�ȣ�(3)�ϸ��ѻ��̶ȵĻ�����ѻ�2D����Ϊ�ͼ�ȩ��������֬Ӧ�á����Ļ��������Ͻ�����һ�����ķ�����
һ������
(һ)�ͼ�ȩ������֬��������״
��ǰ����ǿ��֯Ʒ����ӹ������ڴ��㣬�����Ƿ�֯��ҵ������������⡣��֬���������е�һ����Ҫ���档���ڣ�������Ӧ������������֮һ�Ƕ��Ǽ����ǻ���ϩ��DMDHEU(���2D)���ø��������������֯�ﵯ�Ըߣ�ǿ����ʧС���Ի���Ⱦ��Ⱦɫ֯�����ɹ�ζ�Ӱ���С��������ǿ
�ȵͣ��ͷż�ȩ����[1��2]��֯���Ϻ��й���ļ�ȩ������ζ���ţ����һ�������ijЩ�˵�Ƥ��������[3��4]��
�����������⣬���Ǵ�������������о���һ����Ľ��������գ���һ���濪�����͵���֬���������磬��ȩ��������
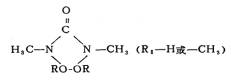
���ķ�Ӧ���ܱȽϵͣ�����Ч����2D��Ľ�2D��֬����һԪ�����Ԫ�����ѻ������õ��ѻ�2D��֬����������֬������֯����ͷż�ȩֵ��ͣ����������[5]�������Ʒ�Ѿ���Ϊ��Ʒ����������֯�����֬������������BASF��˾��Fixapret COC��Fixapret 2348������Cyanamids��
˾��Aerotex Reactant 24��Aerotex Reactant 25�ȡ�
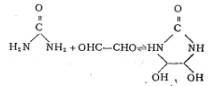
���ѻ�2Dͨ����ʾΪ��
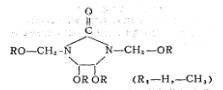
����֪��2D�����е��ĸ��ǻ������봼�����ѻ���Ӧ����������ά�ط���������Ӧ������ͬ��λ�÷�Ӧ���Բ�ͬ��������ǻ��ķ�Ӧ���Խϸ�[7]�����ԣ��ѻ�����IJ�ͬ����Ӱ��������������֯������ܡ����ǡ���ĿǰΪֹ��û�м����ⷽ����о������������о�����Ҫ���ݼ�Ϊ�ѻ�״����������֯�����ܵ�Ӱ�죬���������Ͻ���һ���Ľ��͡�
(��)�ѻ�2D���Ʊ�����������
1��2D���Ʊ���
2D�������������ȩ��Ӧ�ȵõ����Ǽ��٣����ڼ�������������ȩ���ö��õ�2D��֬[8]��Ҳ�������ء��Ҷ�ȩ����ȩ�����һ�������������������·�Ӧһ��ʱ�䣬Ȼ����ǿ���������·�Ӧ����������Һ�����ԣ��õ�2D[9��10]���������ַ������õIJ��ǰ��ת���ʺܵͣ����߸�����϶�[11]��J.Y.Johnson���������Ҷ�ȩ�����������·�Ӧ�õ����ǻ���ϩ��(DHEU)�������ȩ�ڼ��������·�Ӧ�������м���DHEU�Ƿ��ᴿ�����ܵõ��ߴ��ȵ�2D[11��12]����Ӧ�������£�
|
|
|
2��4,5-�ѻ�2D�ĺϳɣ�
�ý��������ӽṹΪ��
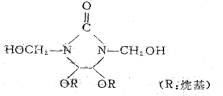
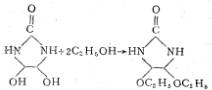
1962�꣬Hideoseki����ͨ������ķ�Ӧ���õ�1,3-���Ǽ�-4,5-����������ϩ���٣������ŷ���������Ǽ���ϼ�ȩ12.0%(����ֵ12.8%)[13]��
|
|
|
3������ѻ�2D�ĺϳ�:
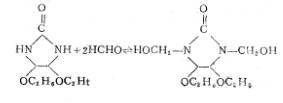
����ѻ�2D���ѻ��ڲ���ͻ��϶����ܷ���������ͨ����2Dˮ��Һ���Ũ����������ǿ�����������봼��Ӧ�õ���[14��15]��
����ʵ ��
(һ)��֬�ĺϳ�
1��2D�ĺϳ�
(l)DHEU�ĺϳ�:
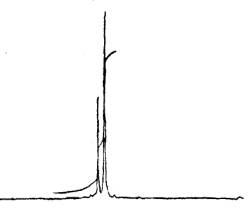
ȡ��Ħ�������������Ҷ�ȩ�������»�Ͻ������ܽ⣬��pH=3.8-4.4��45��55������Ӧ3-4Сʱ���кͽᾧ�����۵�ܲ����۵�Ϊ133-134.5��������ֵΪ133-135��[16]���ÿ��������ú�����Ϊ23.62%������ֵΪ23.73%�����۵�ͺ��������Խ�������Զ϶�����������DHEU��Ϊ�˽�һ��֤ʵ�ֶԸþ��������NMR��������D2O���ܼ��������е�ԭ�Ӻ���ԭ���ϵ��ⱻ������ȡ����ֻʣ�»���̼ԭ���ϵ���ԭ�ӣ�ͼ1������NMR��ͼ��
|
|
|
ͼ 1 |
��ͼ�п��Կ�����ֻ����������壬��=4.62�ķ������⽻����ˮ�����е����ӹ���壬����֮�⣬��ֻ����=4.85�������ӹ���塣��������ͼ��4,5-����������ϩ���NMR��ͼ(ͼ2)��Ƚϣ����Ե�֪�����弴Ϊ����̼ԭ�������ӵĹ���塣��ˣ����Կ϶���������Ӧ���þ�����DHEU��
(2)DHEU���Ǽ���:
��ȡһ������DHEU������Ħ����ΪDHEU�����ļ�ȩˮ��Һ����pH=7-8���¶�45-50������ӦԼ3Сʱ����ȴ�����£�
����pH��7.0���õ�������Ϊ56.3%����֬ˮ��Һ������һ������ˮ���40%ˮ��Һ����ΪR-1��
2��4,5-�ѻ�2D�ĺϳ�:
(1)4,5-����������ϩ��ĺϳɣ�
ȡ118��DHEU��460����ˮ�Ҵ���Ϻ���pH=l-2.3��50-60������Ӧ1Сʱ����ȴ�����£��ü�������ԣ����˳������Σ���Һ��0-4�����ü��ɵõ���״���塣�����þ�����������ˮ�Ҵ������ؽᾧ���þ�����l57-160���ۻ�������ֵ159-160��[13]�����߱ȽϷ��ϣ�ֻ��ʵ��ֵ�۳̽ϳ���Ϊȷ�жϸþ����Ƿ�Ϊ�����4,5-����������ϩ�壬����NMR��ͼ(��D20���ܼ�)��ͼ2��
|
|
|
ͼ 2 |
����ͼ�п��Կ�����������ԭ�ӽ��û���ֻ����-CH3��-CH2��-CH�����ӹ���壬�����ŵ����ӹ������ָ߶ȱ�ֵ�������������-CH3��-CH2-����HC-���������ı�ֵ��ȣ�
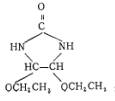
���Կ϶��þ���ȷΪ4,5-����������ϩ�塣
|
��ѧλ�� |
1.08 |
3.52 |
4.76 |
|
���ָ߶�(��) |
36 |
25 |
12 |
|
���ָ߶ȱ�ֵ |
3 |
2 |
1 |
|
���� |
-CH3 |
-CH2- |
��HC- |
(2)4,5-����������ϩ����Ǽ�����
ѡ��4,5-����������ϩ�����ȩĦ����Ϊ1�U2����pH=9-10��40-45������Ӧ3Сʱ��Ȼ����ȴ�������кͣ�����һ������ˮ���40%ˮ��Һ����ΪR-3��
3������ѻ�2D�ĺϳɣ�
��R-lˮ��Һ����Ũ��������һ��������ˮ�Ҵ�����pH=1.4-1.6��38-40������Ӧһ��ʱ�����ȴ�����£��кͣ���ȥʣ����Ҵ������40%ˮ��Һ����ΪR-3��
(��)��֬��Һ�ķ���
�ⶨ����֬ˮ��Һ�е������ȩ[16]����������֬��Һ��Ʒ��50-55����ո����ͿĤ����IR��ͼ����Fixapret COC�����ѻ�2D������NMR���á�
(��)��֬����
֯��:33��33����ƽ��������ë��������Ư�ס�˿��ǰ����������ǰ��2��/������ϴ�ӣ��پ�ˮϴ���Խ���֯���ϱ����ļ��ԡ�
����:
�ѻ�2D��֬(��/��) 59
(2D 45��/��)
MgC12 6H2O(��/��)�� 14
������(��/��)�� 0.7
JFC(��/��)�� 1
��������:
��������(��Һ��70%)��Ԥ��(100����1��30")������(17O����1��) ����ϴ����ˮϴ��������ˮϴ�����ɡ�
(��)������֯�����ܲ���
����ǿ��������GB3923-28�����Խ���Ե�ɴǿ����ʾ[17]��
˺��ǿ����GB3919-83���η�[18]��
����ظ���:GB3819-83[19]
������:AATCC92-180[20]��
�ͷż�ȩֵ:GB2912-82A��[21]
֯���Ϻ�������Kjeldahl��[22]
�������������
��һ������֬�ĺ�����ͼ�������ṹ����
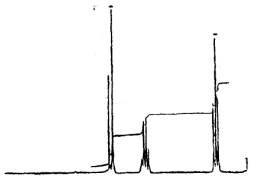
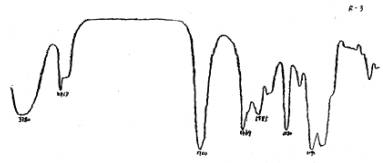
ͼ3��R-l�ĺ�����ͼ������Ҳ����������������Ʒ2D��IR��ͼ�����ҽ����˷�������Ϊ��2D����ͼ����ͼ4[24]��ͼ3��ͼ4��
|
|
ͼ3
|
|
|
|
|
ͼ4��a�� |
ͼ4��b�� |
ͼ4��c�� |
ͼ4(a)���Ǽ����ǻ���ϩ��(����¹�CPN)
ͼ4(b)���Ǽ����ǻ���ϩ��(�ձ�CPN)
ͼ4(c)���ؼ���Ь����ϩ��(����CPN)
�Ƚϣ����Է������ǻ���������ͬ�ģ�˵�����ǵķ��ӽṹ������ͬ�����Ʊ����̿��ǣ�J.Y.Johnson��������ͬ�ķ�Ӧ�����õ���2Dˮ��Һ���������롢����õ�2D���塣Ԫ�ط��������C=33.62%��H=5.93%��N=15.96%(����ֵ C=33.71%��H=5.618%��N=15.73%)���۵㣻86��[12]���ڱ�ʵ���У�����û�н������ķ��룬�����ڷ�Ӧ������ͬ���ٽ��IR���ã������Ʋ�R-1��Ҫ�����2D��
ͼ5��R-3��R-5��Fixapret COC��IR��ͼ�����Կ�������2D��IR��ͼ��ȣ���������2993��2962����-1��1385��1340����-1��1075��1100����-1�������շ壬���������շ�ֱ���-CH���е�C-H��չ��������C-O-C����չ�����շ�[22]��ͬʱ�������������������շ�(1700��1725����-1��1470��1490����-1��1230��1250����-1)������Ӧ���ƶ�������֮�⣬û�������仯��˵��������2D��ȣ���ĸ��ṹ��û�з����ܴ�ı仯��ֻ�ǻ����ٵط����˹����ŵı仯��Ҳ�����ǻ����ѻ���
R-3����4,5-����������ϩ�����ȩ�ڼ��������·�Ӧ�õ��ġ��ڸ������£��Ѽ��Ǻ��ȶ��ģ����ᷢ���ֽ⣬��ȩ��Һ�д��ڵļ״�Ҳ�������ǻ�������Ӧ����ˣ�R-3�϶���4,5-��������������ͪ���Ǽ��������ԭ���������������ı�ֵΪ1:1��
�Ƚ�R-3��R-5��IR��ͼ�����Կ�
|
|
|
|
|
ͼ 5 |
����1075��1100����-1�������շ�ǿ�ȣ�R-5��Ȼ����R-3��˵��R-5�е�������������R-3��������3400����-1���������շ壬�����Դ���-OH��NH ��˿��Դ��Ե������Ʋ�:R-5�еĵ������������ı�ֵ����1�U1��1�U2֮�䡣
S.L.Vall�о���2D�����в����뻷���ǻ��ķ�Ӧ���ԡ�˵�������Լ�Ϊ�״���ˮ������С����ʱ��2D�������ĸ�λ�õ��ǻ���������ķ�Ӧ������ȣ��������Լ����ӽϴ�ʱ(�������)���뻷�ϻ��ŵķ�Ӧ�Խ��͡���ԭ����������������ϰ��Ĵ��ڡ�����ѡ���Ҵ������Լ������Ӵ�С���ڼ״��������֮�䡣�ѻ���Ӧ��λ�ò���ȷ��������ϵ��ѻ��̶ȿ��ܱȻ��ϵ��Ը�һЩ��
(��)������֯������ܲ��Խ��������
|
|
��ɴ����ǿ��(N) |
˺��ǿ��(N) |
����ظ���(��+γ������)(��) |
����% |
�ͷż�ȩ��ppm�� |
|
R-1 |
0.106 |
0.80 |
249 |
62.4 |
295 |
|
R-3 |
0.133 |
0.92 |
220 |
77.5 |
137 |
|
R-5 |
0.120 |
0.92 |
224 |
11.4 |
329 |
|
Fixapret COC |
0.134 |
1.0 |
241 |
6.21 |
174 |
|
�հ� |
0.271 |
2.3 |
154 |
2.4 |
- |
1���ӱ��п��Կ������ѻ�2D�������֯���ǿ������2D�ߣ�������ȴ�ϵͣ�������4,5-�ѻ�2D������֯���Ϊ������������������ѻ�2D��Ӧ���Խ��͵�ԭ��Ϊ��֤ʵ���ǵ��Ʋ⣬�ⶨ��֯����������ˮϴ��ĺ����������Խ������:
��֬ R-l R-3
������(%) 0.586 0.477
��������֬����Һ�У����ߵ�Ħ��Ũ�Ȼ�����ȣ�֯���Ϻ������Ķ��ٷ�ӳ�˽���������ά�ط�Ӧ���ܵĸߵ͡���Ӧ����Խ�ߣ�����������ά�ط�Ӧ�γɵĽ���Խ�࣬֯���ϵĺ�����ҲԽ�ߡ���ˣ�R-3����ά�صķ�Ӧ���ܱ�R-1�ͣ���DMDHEU�л����ǻ������ѻ�ʹ�������ķ�Ӧ���Խ��͡�
2��R-3��R-1��ȣ�R3�������ߣ������������������ԭ������ġ�һ����4,5-�ѻ�2D����ά�صĽ�����Ӧ���Խ��ͣ������2D����ά�صĽ�����Ӧ����δ������Nһ�Ǽ��϶࣬��
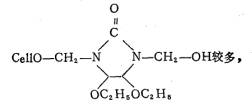
��Ưʱ�������࣬�����������[24]���䷴Ӧ�������£�
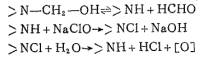
(�ͷų�������������ά�صĽ���)����һ��ԭ����������ԭ��������������ֱ�ӽ�����Ӧ[2]��
|
|
|
|
HCHO+ROH+HCl |
|
|
|
������Ӧ�������뵪ԭ���ϵĵ������ܶ��йأ��������ܶ�Խ�ߣ�������Ӧ����Խ�ߡ�4,5-�ѻ�2D����ά�ؽ����γɵĽṹΪ��
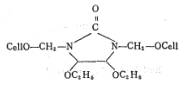
��2D�γɵĽ�����Ƚϣ��һ����й�������;ʹ��
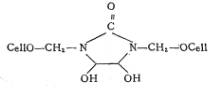
��ԭ���ϵĵ������ܶ��������ȵ��û���Ӧ������ߣ�����Ƚ������γɣ�N-Cl��ʹ���������ߡ�
R-5����֯�������ܵ͡���R-3��֬�������Է�������ó���DMDHEU�����ǻ����ѻ�ʹ�������ߡ�����R-5��֬�����������R-5�б�Ȼ���ڻ����ǻ����ѻ���������ʹ�������ߵ����ء�ʵ��Ľ��ȴ������dz��ͣ�˵����R-5�б�Ȼ����ʹ���͵����ء�R-5��R-l��R-3�IJ�֮ͬ�������Ǵ��ڲ�����ǻ������ѻ������������͵�ԭ��ֻ�ܹ���ڲ�����ǻ����ѻ������ԣ�2D��1,3-λ���ѻ��ɽ�������
3��������֯���ͷż�ȩ����:�ú���ȩ��������������֯���ͷż�ȩ����Ҫ��Դ���ǵ��˷�Ӧ������[24]���ڲ��Թ����У�����������ά���γɵĽ���Ҳ�ܷ���ˮ�⣬�ͷų���ȩ[26]��
�ӱ��п������ѻ�2D����֯����ͷż�ȩֵ����2D������R-5Ϊ��͡� R-3������֯����ͷż�ȩ��2D�ͣ�������ά���γɽ�����Ľṹ���£�
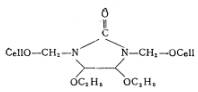
Rolf Zeidler��Ϊ2D����ά���γɵĽ���������������Ӧ��
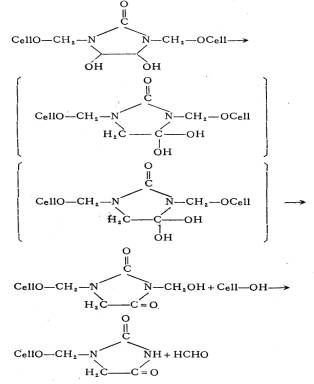
4,5-λ�Ͼ�Ϊ�ǻ�ʱ���������ǻ��Ļ�λ��Ӧ���γɲ��ȶ����м��壬ת��Ϊ����ά�ؽ������������塣���ֻ�����ṹ�IJ��Գƣ�����������ˮ���ȶ��Է����仯����Ҫԭ��4,5-λ���ǻ���������ȡ������ֹ��תλ��Ӧ�ķ�������Ӧ������˽��������ȶ��ԣ��������ͷż�ȩ��[5]��
R-5�м���1,3-λ�ѻ�������4,5-λ�ѻ���4,5һλ�ѻ�ʹ�ͷż�ȩֵ����,����R-5���ͷż�ȩ����Ȼ�ܵͣ�������˵��1,3-λ�ѻ���֯����ͷż�ȩ����Ӱ�졣
�ӱ��л����Կ�������R-5������֯���������е���ܱ�Fixapret COC���Բ������߶��Ƚϵͣ�R-5�����FixapretCOC���Ը�һЩ�������ͷż�ȩ������ǰ��Ҫ�͵öࡣ
��NMR����,Fixapret COCΪ���ѻ�2D���ɴ˿�֪,���Ҵ���2D�����ѻ����Եõ��ͼ�ȩ������֬����������֯������ܿ���״��ѻ���Fixapret COC��������
�ġ�����
1���������Ҵ�����״���ΪDMDHEU���ѻ���,ѡ�����˵ĺϳɷ���,�õ��ͼ�ȩ��ͼ�ȩ������֬��
2��4,5-���ѻ�����ά�صķ�Ӧ���ԣ���2D����ά�صķ�Ӧ���Խ��ͣ���4,5-���ѻ�2D�������������֯�������ǿ�ȣ����ɽ����ͷż�ȩ����2D��1,3-λ�ǻ������ѻ����������������֯�������ǿ�ȡ�
3���ϸ��ѻ��̶ȵĻ�����ѻ�2D�������֯�������ԽϺã��ͷż�ȩ���ܵ͡�
�������������ȡ���������λ��ʦ��ָ������ɵģ��ڴ˱�ʾ���ĵظ�л��
�����
[1] Menachem Lewin Stophen B.Sello,��Handbook of Fibers cience and Technology:volume�� chemical Processing of Fibers and Fabrics Futional Part A��,New York,l983
[2]H.������,����֯��Ļ�ѧ������,ˮ������,��֯��ҵ�����硣
[3]�����顢ׯ��ϼ,��ӡȾ��1979��,��4��,23ҳ
[4]������,��ӡȾ��,1979��,��4��,47ҳ��
[5] Dr.Rolf ZeidIer,��The Formaldehyde ProbIem in Textile Finishing��.
[6] Pamela J.Jaco,and James E.Hendrix��T.C.C��,14,9,54һ(1982)
[7] S.L.Vail,��T.R.J��,44,5,400-1 (1974)
[8] U.S.Patent 2,876,062
[9] U.S.Patent 4,016,335(1977)
[10] U.S.Patent 3,903,033(1975)
[1l] Br.Patent 720,386
[12] Br.Patent l,032,379
[13] U.S.Patent 3,029,164(1962)
[14] Br.Patent l,118,515(1968)
[15]�ձ���������,��47-35358
[16] Sidney L.Vail,Robert H.Barker,and P.Gury Mcnnitt,��J.Org. chem.��,30,2179-(1965)
[17] GB 3923-28
[18] GB 3919-83
[19] GB3819-83
[21] GB 2912-82
[22] ��ҫ��,���л�������,�ߵȽ���������,1981
[23] ������,��ӡȾ��,1984��,��5��,31ҳ
[24] Sello S.B,��T.C.C��,14,11,9-15(1982)
[25] Sidney L.Vail,"Current Trends in Finishing Fabrics with Low Formaldhyde Release Properties"
[26] B.A.Rottes Andrews,and R.J.Harper,��J.T.R��,50,3,177-(1980)
[27] Sidney L.Vail,Jacquelies M.Simeneaux,and Zhou Xiang,��A.D.R��,71,9,62-(1982)