���ԭ���Ʊ�ʯīϩyd20227
��˧���A��ʤ��κ���壬������* �ൺ�Ƽ���ѧ ���ܲ����빤�̽������ص�ʵ���ң�ɽ�� �ൺ 266042
�ո����ڣ�2015-08-19
������Ŀ��������Ȼ��ѧ������Ŀ(51373084)���ൺ�н�����ҵ�Ƽ���չר����Ŀ(JK2014-4).
����飺�� ˧(1989��)���У�˶ʿ�о���. *ͨ����ϵ��.
ԭ�أ��ൺ�Ƽ���ѧѧ������Ȼ��ѧ�棩2016
��ժҪ�����ü�������������䷨��ԭ����ʯīϩ(GO)���Ʊ���ɢ�����õ�ʯīϩ(RGO)ˮ��ɢҺ���о���3�ֲ�ͬ��ԭ��(�����ǡ����⻯�ơ��ȼ���ά��)�Ļ�ԭЧ������֤����������仹ԭGO�ķ�Ӧ�������Է�Ӧ����������-�ɼ����չ���(UV-vis)������ɢ�����(Raman)��X-��������(XRD)�Ȳ����ֶν����˱����������������������������Ч�ؽ�GO����ĺ������Ż�ԭ���Ʊ�����ʯīϩ��ɢ�����ã��ɾ��ȷ�ɢ��ˮ��Һ�в����Ա����ȶ�״̬��3�����ϣ���Ч�ؽ����ʯīϩ����ɢ���ܼ��е�ȱ�㡣
���ؼ��ʡ� ʯīϩ�� �����ǣ� ���⻯�ƣ� �ȼ���ά�أ� ���ԭ
����ͼ�������TB 321 ���ױ�־�룺A ���±�ţ�1672-6987(2016)06-0631-06��DOI��10.16351/j.1672-6987.2016.06.008
ʯīϩ�ǵ���̼ԭ�ӽ��ܶ������ɵĶ�ά�䳲����ṹ��ƽ�污Ĥ����[1]��2004��GEIM���״γɹ�������ȶ���ʯīϩ[2]������ʯīϩ����Ľṹ����һϵ�������������ѧ���ܣ�ʹ���ڶ̶̵ļ���ʱ�����Ϊ�����ײ��Ͽ�ѧ�о����ȵ�[3]���������������������ӡ��������塢���ܲ��ϡ����ܲ��Ϻ��ϲ��ϵ�����չ�ֳ�������Ӧ��ǰ��[4-5]��
ʯīϩ���Ʊ������ܶ࣬�ɷ�Ϊ���������ͻ�ѧ����������������Ҫ����е���뷨[2]�������и[6]����ѧ������Ҫ���Ƚ�SiC��[7]����ѧ���������[8]������-��ԭ��[9]���Ƚԭ��[10]�ȡ�������½�������˶������͵��Ʊ�����������Һ����뷨[11]���绯ѧ��ԭ��[12]����绹ԭ��[13-14]���л��ϳɷ�[15]������̼���Ϻϳɷ�[16]��������[17-18]�Ⲩ����ķ���[19-20]�ȡ�
����-��ԭ���Ǵ��ģ�Ʊ���Ӧ��ʯīϩ�Ŀ��з���֮һ����ѧ��ԭ����ʯīϩ��һ�ַdz���Ч���Ʊ��������Ҿ��з�Ӧ�����º͡��ɱ��͡��ܺĵ͵��ŵ�[21]�����ǻ�ѧ��ԭ��ʹ�õĴ���������ˮ�������������ȣ����ж��Ժ��Ȳ��ȶ��ԣ�����������Ӧ��[22-23]�����ڣ�ZHANG��[24]������23 ���������£���ά����C��������ʯīϩ(GO)��ˮ��ɢҺ�У��Ʊ���ˮ���ԺõĻ�ԭʯīϩˮ��ɢҺ������һ����Բ��������ж��һ�������Ⱦ���Ʊ���������������ʵ��ʱ��(48 h)�����Ļ�ԭ������������ʵ�ʵ�Ӧ�á�
�������仹ԭ�Ʊ�ʯīϩ��������������£�������ʯīϩ��ˮ��ɢҺ��ԭ��ʯīϩ��ˮ��ɢҺ[25]���÷�������������������뵼�幤�յĹ�̹��ռ��ݣ�������ڽ�ʯīϩӦ�õ�����������˵���зdz���Ҫ������[26]���������ԭ�Ʊ�ʯīϩ�Ĺ�����û���к����ʲ�������ɫ���������ظ��Ժã��Ʊ����ڶ̣��õ�ʯīϩ��ˮ��ɢҺ������ֱ������Ϳ�ϵ�ˮ�Բ����У���������о���Ա������о���Ȥ��
AKHAVAN��[27]��TiO2Ϊ����������������»�ԭ�Ʊ�ʯīϩ��MATSUMOTO��[28]��H2��N2��������������ԭ�Ʊ�ʯīϩ�����ڵ��о���Խ��١��������Ӳ�ͬ�Ļ�ԭ��ϵ���֣������ԭʯīϩ����һЩ����������̽�����о���
1 ʵ�鲿��
1.1 �Լ�������
����ʯī(GO��SGO-202A)���Ƚԭʯīϩ(TrG��SGN-102)���ɶ�ϩŵ�²��ϿƼ�����˾��һˮ�����ǣ�����й⸴�Ƽ���չ����˾���ȼ���ά��(CMC)�����������ѧ�Լ�����˾�����⻯�ƣ��Ϻ����ջ����Ƽ�����˾��ʮ�������������(SDBS)���Ͼ����û�������˾��Ũ���ᡢ���ᡢ���ᡢ�������Ϊ���ۣ�ֱ��ʹ�á�
��������ϴ����KQ-50B�ͣ���ɽ�г�����������˾������ʽ�����(����254 nm)��WFH-204B�ͣ�������Ȫ�˹��������˾��˫��������ɼ��ֹ��ȼƣ�TU-1901�ͣ���������ͨ�������������ι�˾����������ǣ�TGA-IR Vertex70�ͣ��¹�Bruker��˾��X����������(XRD)��D-MAX 2500/PC�ͣ��ձ���ѧ��˾���������������ǣ�InVia�ͣ�Ӣ��Renishaw��˾��
1.2 ����ʯīϩ(GO)��Һ���Ʊ���Ũ�ȵ�ȷ��
��ȡһ�������ĸ�������ʯī(GO)�����ձ��У����ձ��м�������ȥ����ˮ(���Ƴ�1 mg��mL-1��GOˮ��Һ)�����ձ����볬������ϴ���г�����ɢ��Լ2 h���õ������ȶ���ɢ����Һ��
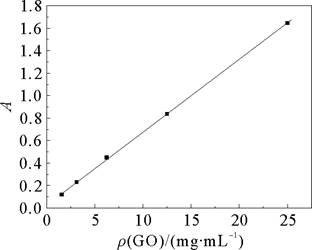
����ʯīϩ��Һ��Ũ�ȿɸ����ʲ��ȶ�����ȷ������ͼ1�����Բ���225 nm����ͼ1�õ�GOŨ�Ⱥ�����ȵ����Է��̣�y=64.668x+0.030 1��
|
|
|
ͼ1 ����ʯīϩ(GO)���ʲ��ȶ����� |
2 ���������
2.1 ���������ʱ���GO��ԭЧ����Ӱ��
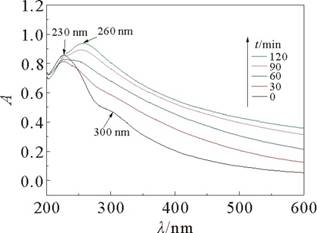
������ʯīϩˮ��ɢ��Һ(1 mg��mL-1)������������Բ�������������չ��IJⶨ�������ͼ2��
�������չ����У�230
nm����ǿ���շ���������ʯīϩ�IJ�����C![]() C���С���*ԾǨ������ģ�����300 nm���������շ����ɲ�����C
C���С���*ԾǨ������ģ�����300 nm���������շ����ɲ�����C![]() O��n����*ԾǨ�������[28]����ͼ2���Կ���,������������ʱ����ӳ�����ԭ�������ʯīϩ(RGO)��230 nm���������������Ƶ���260 nm���Ҳ���������������ߣ���������C
O��n����*ԾǨ�������[28]����ͼ2���Կ���,������������ʱ����ӳ�����ԭ�������ʯīϩ(RGO)��230 nm���������������Ƶ���260 nm���Ҳ���������������ߣ���������C![]() C���ŷ������Ĺ������õ��������շ�ĺ��ƣ���˵������ʯīϩ��sp3�ӻ��ṹ����ԭ��ʯīϩ��sp2�ӻ��ṹ�õ��˻ָ���������������ʱ����ӳ���GO��300 nm���ļ����������60 min����ʱ�÷���ȫ��ʧ����������ʱ��Խ����Һ�����շ��ֵԽ�ߣ�������Һ�������Խ�ߡ�300 nm�������շ���ʧ������C
C���ŷ������Ĺ������õ��������շ�ĺ��ƣ���˵������ʯīϩ��sp3�ӻ��ṹ����ԭ��ʯīϩ��sp2�ӻ��ṹ�õ��˻ָ���������������ʱ����ӳ���GO��300 nm���ļ����������60 min����ʱ�÷���ȫ��ʧ����������ʱ��Խ����Һ�����շ��ֵԽ�ߣ�������Һ�������Խ�ߡ�300 nm�������շ���ʧ������C![]() O����ʧ�����һ��֤����RGO�еĺ���������ʧ��������ʯīϩ�õ���ԭ���Ʊ���ˮ�з�ɢ�����õ�ʯīϩ��������������ǿ�Ƚϵͣ�˵���仹ԭ��ʯīϩ��Ũ�ȱȽϵ͡�
O����ʧ�����һ��֤����RGO�еĺ���������ʧ��������ʯīϩ�õ���ԭ���Ʊ���ˮ�з�ɢ�����õ�ʯīϩ��������������ǿ�Ƚϵͣ�˵���仹ԭ��ʯīϩ��Ũ�ȱȽϵ͡�
|
|
|
ͼ2 GO���������չ��� |
2.2 �����Ƕ�GO��ԭЧ����Ӱ��
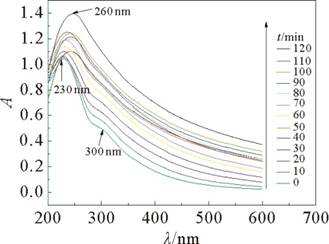
��������(C6H12O6)Ϊ��ԭ����GO�������ԭ������ʯīϩˮ��ɢҺ��Ũ��Ϊ1 mg��mL-1��m(GO)��m(C6H12O6)=1��4�������ͼ3��
|
|
|
ͼ3 GO/�����ǵ��������չ��� |
��ͼ3���Կ�������������ʱ����ӳ�����ԭ�������ʯīϩ(RGO)��230 nm���������������Ƶ���260 nm���Ҳ���������������ߣ���˵��ʯīϩ�Ĺ���ṹ�õ��ָ���������������ʱ����ӳ���GO��300 nm��������������������60 min����ʱ�÷���ȫ��ʧ����˵������ʯīϩ�Ѿ�����ԭ���Ҵ�ͼ2��ͼ3�Ա��п��Կ�����ͬGOŨ���£���ԭ������ϵ��������������ǿ��ֻ��0.96�����������ǻ�ԭ����ϵ����������ǿ�ȴ���1.4������˵����������ǿ��GO�Ļ�ԭ�̶ȣ�������GO�Ļ�ԭ��
2.3 ��ԭ�������������Ի�ԭЧ����Ӱ��
��ͬ���������Ƕ�GO��ԭ����������ͼ4����ͼ4�п��Կ����������ǵ������Ի�ԭЧ����������Ӱ�죬�����������120 min GO����ĺ������Ŵֶ���ʧ������ʯīϩ�Ĺ���ṹ���õ��ָ������������DZ���������RGO������Ȳ������ߣ���GO�������������ȴﵽ1��4ʱ����ȵ�����ߣ�˵����m(GO)��m(������)=1��4ʱ��ԭЧ������õġ�
|
|
|
ͼ4 GO/�����ǵ��������չ��� |
2.4 �������չ��ṹ����
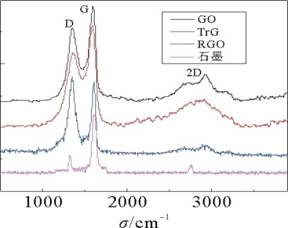
ͼ5��ʯī������ʯīϩ(GO)���Ȼ�ԭ����ʯīϩ(TrG)�����������ԭ����ʯīϩ(RGO)����������ͼ���߶������ʯī��Raman������һ�����2���壬һ����ΪG��(1 596 cm-1����)��G����̼sp2�ṹ�������壬��ӳ��Գ��Ժͽᾧ�̶ȣ������խ��ǿ�ȸߣ�˵��̼ԭ�Ӿ����������Žṹ��sp2�ӻ�ռ�������ᾧ�̶ȸߣ���һ����ΪD��(1 329 cm-1����)��D��ͨ������Ϊ��ʯīϩ�������壬D����ʯī�ľ����ijߴ������ȱ���й�[29]��D��Ĵ��ڣ�˵��ʯī�д���һЩȱ�ݺ�sp3�ṹ��[30]����ͼ5��GO���߿��Կ���������3���壬�ֱ���D��(1 329 cm-1)��G��(1 596 cm-1)��2D��(2 810 cm-1)��2D��ķ���״���߿���λ��ֱ�ӷ�ӳ��ʯīϩ���Ӵ��ṹ������Щ���Ӵ��ṹ��ʯīϩԭ�Ӳ����й�[31]����ʯī��Ƚϣ�����ΪG�������D���������ǿ����������ʯī����������ʯīƬ����̼ԭ���뺬���������ᣬ��������sp3�ӻ���ʽ�ɼ����������ṹ��̼ԭ�ӣ�ʯī����ĶԳ��Լ������������ܵ��ƻ���TrG��RGO�����������ж�������G�������D���������ǿ��ԭ��������ʯīϩ��ԭ�IJ���ȫ������������ԭ������ԭ��ʯīϩ�������Ա�Ȼ���ӣ��ƻ���ʯī����ĶԳ��Ժͳ��������ԡ�
|
|
|
ͼ5 GO��TrG��RGO���������� |
2D�������һ��˫����˫������̣���ʯīϩ���ܴ��ṹ�������[32]��2D��ķ��ͺ���ǿ�����ƶ�ʯīϩ�IJ�������ǿԽ������ʾʯīϩ�IJ���Խ�١���TrG��RGO�������չ�����ͼ�����ó���TrG��2D��������ԣ���ǿ�Ƚϸߣ�˵��TrG���к��ٵ�ʯīϩ��������RGO��2D�岻���ԣ����ܵ�ԭ���ǣ���ԭ�õ���RGO����Գ��Ժͳ��������Ա��ƻ�����ԵЧӦ���ӣ�ȱ�ݽ϶࣬����˫����˫����������⣬2D�������
ͨ����GO��RGO�������չ����״�����������D���G��ǿ�Ƚ��бȽϣ���ID/IG�ı�ֵ�ֱ�Ϊ0.92��1.09��ID/IG���������������ײ��ϵ�ʯī���̶�[33],ID/IGԽ���ʾʯīϩ��������Խ��[30]�������ϣ���GO����ԭ��ʯīƬ�ϵĺ��������ű���ȥ��sp2̼����ṹ������̶Ȼ����ӣ�sp2���������ID/IG���½��������ԵĽ��ΪRGO��ID/IGֵ��GO�ĸߣ����ܵ�ԭ���ǣ�GO����ԭ������sp3�ӻ�̼ԭ�������������γ��µ�sp2�ӻ����������γɵ�sp2�ӻ������GO��sp3�ӻ�����С�����ʹ��ԭ���ʯīϩ������ߴ��С����������࣬����������ID/IG�ı�ֵ���ߡ�
2.5 X��������(XRD)����
����XRD�����������ԭ��ʯīϩ���Ȼ�ԭʯīϩ���б����������ͼ6����ͼ6����a�ɿ��������������ԭ��ʯīϩ2����22�����ң���һ�����ͽϿ�������壬�������ǿ�Ƚ��������ݲ�����2dsin��=n��(����n=1����=0.154 nm)���Լ���ó�ʯīϩ����ԼΪ0.41 nm��
|
|
|
ͼ6 RGO��TrG��XRD��ͼ |
��ͼ6����a������b���бȽϿ��Կ��������ַ����Ƶõ�ʯīϩ��XRD���շ��λ�ñ仯����֮ͬ�������Ƚⷨ�Ʊ���ʯīϩ������Ƚ�������Һ���Ʊ���ʯīϩ������Ƚ�����ƽ����˵�����ַ����Ʊ���ʯīϩ��������һ�£������ԭ�����Ʊ���ʯīϩ��Ƭ��֮��������Ը���һЩ��Ҳ���ǰ����ɢ�̶ȸ���һЩ����Ҳ��2.4���������ķ������Ǻϡ�
2.6 ��ͬ��ԭ���Ļ�ԭЧ��
Ϊ�˶Ի�ԭЧ���������ۣ�ѡ����3�ֲ�ͬ�Ļ�ԭ���������������õ��������Լ����º͵Ļ�ԭ�����Լ����������ɵĻ���������ʹ���Ϊһ������Ļ�ԭ�����ȼ���ά����(CMC)��һ��������������ά������ĸ߷��ӣ�������ˮ���γɾ���һ���ȵ�����Һ��������ά��ʯīϩˮ��ɢҺ���ȶ��ԡ������������⻯��(BH4Na)���Ե��룬���н�ǿ�Ļ�ԭѡ���ԣ�������Ч�ػ�ԭ�ʻ���ȩ���������ϳɺ��л��ϳ��ж�����������ԭ������ˣ�ѡ����3�ִ����ԵĻ�ԭ�Լ������ԭ��Ч�������о�����1Ϊ��ͬ��ԭ�������Ż���ԭ������
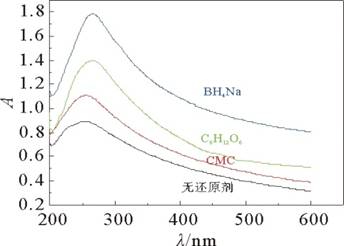
��ͬ��ԭ�����������չ���ͼ7����ͼ7���Կ�����û�����ӻ�ԭ��������ʯīϩ��������ǿ�ȵͣ�����ԭ�ij̶�С����ԭ����ʱ�䳤�����ۺϻ�ԭЧ�����ۺϻ�ԭЧ����õ������⻯�ƣ����������ԭ��CMC�Ļ�ԭЧ���Ƚϲ�����ø÷����Ʊ���ʯīϩ��ˮ���ķ�ɢ�ȶ������(��1)����ԭҺ�����ȶ����21 d���ϡ�ԭ����CMC��Һ�������������ʯīϩ��ˮ��Һ�еķ�ɢ�ȶ��ԡ�
|
��1 ��ͬ��ԭ�������Ż���ԭ���� |
|
|
��ԭ��������������ʱ��/minm(GO):m(��ԭ��)RGO��ɢҺ���ȶ�ʱ��/d���⻯��601��4.02��3������1201��4.02��3CMC1201��1.5>21��ԭ��12002��3
|
|
|
ͼ7 ��ͬ��ԭ�����������չ��� |
���ԭ�Ļ�����[28]��ˮ�������������·������룬������ˮ�ϵ���![]() ��ˮ�ϵ���
��ˮ�ϵ���![]() ��ǿ�Ļ�ԭ�ԣ�������GO������ԭ��Ӧ����GO��ԭΪRGO��ˮ�ϵ����ǻ�ԭ��Ӧ����������Ҳ����˵ˮ�ϵ��Ӳ������ٶȺ�������Ӱ�쵽��Ӧ�Ŀ����ͳ̶ȡ���ʹ�����⻯��Ϊ��ԭ��ʱ�����⻯����ˮ��Һ�з������룬�ӿ���ˮ�ϵ��ӵIJ����ٶȡ�������ˮ�ϵ��Ӳ�����������ʹ��ԭЧ��Խ��Խ�á�
��ǿ�Ļ�ԭ�ԣ�������GO������ԭ��Ӧ����GO��ԭΪRGO��ˮ�ϵ����ǻ�ԭ��Ӧ����������Ҳ����˵ˮ�ϵ��Ӳ������ٶȺ�������Ӱ�쵽��Ӧ�Ŀ����ͳ̶ȡ���ʹ�����⻯��Ϊ��ԭ��ʱ�����⻯����ˮ��Һ�з������룬�ӿ���ˮ�ϵ��ӵIJ����ٶȡ�������ˮ�ϵ��Ӳ�����������ʹ��ԭЧ��Խ��Խ�á�
����ʵ��ԭ����ʵ�����ķ���������������ʱ�䡢��ԭ�������Ϻͻ�ԭЧ���ȷ������������⻯������ѵĻ�ԭ������Ҫ��ǿ�Ʊ�ʯīϩ�ķ�ɢ�ȶ��ԣ����Կ�������ϵ������CMC�������ϵ�����Ա���ʯīϩ��Һ�ij����ȶ���
3 �� ��
�����ǡ����⻯�ơ�CMC 3�ֻ�ԭ�������Բ�ͬ�̶ȵظ�������ʯīϩ��ˮ��Һ�е����ԭ���������Ʊ����ȷ�ɢ��ˮ�е�ʯīϩ��ɢҺ�������ǵ�GO��Һ������Ƚ�ǿ����ԭЧ���Ϻã��������������������ӣ�GO��Һ������Ȳ������ӣ���m(GO)��m(������)=1��4.0ʱ�������߿ɴ�1.4����m(GO)��m(���⻯��)=1��4.0����������ʱ��Ϊ60 min�����������£����⻯�ƻ�ԭ��GO��Һ���������ߣ����õ���RGO�IJ�����࣬��ԭЧ����ã��ȼ���ά����(CMC)��ԭ��RGO�IJ�������͵ģ������������仹ԭ��RGO�ķ�ɢ������õģ������ɢҺ���ȶ���Ҳ����õģ������ȶ����3�����ϡ�
�� �� �� ��
[1] GEIM A K, NOVOSELOV K S. The rise of graphene[J]. Nature Materials, 2007, 6(3): 183-191.
[2] NOVOSELOV K S, GEIM A K, MOROZOV S V, et al. Electric field effect in atomically thin carbon films[J]. Science, 2004, 306(5696): 666-669.
[3] ���䲨, ���ڱ�, ����, ��. ����������ɫ��ԭ�Ʊ�ʯīϩ [J]. ����̿����, 2011(1): 16-20.
WAN Wubo, ZHAO Zongbin, HU Han, et al. Green reduction of graphene oxide to graphene by sodium citrate[J]. New Carbon Materials,2011(1):16-20.
[4] ���ı�, ������, �Խ�. ���ٽ��Ҵ��Ʊ� TiO2/ʯīϩ�����ϲ��ϼ������[J]. �ൺ�Ƽ���ѧѧ��(��Ȼ��ѧ��), 2014, 35(5):489-492.
HU Wenbin, QIN Yulei, ZHAO Jian. Preparation and characterization of TiO2/graphene nanocomposites by supercritical ethanol[J]. Journal of Qingdao University of Science and Technology(Natural Science Edition), 2014, 35(5):489-492.
[5] ³ս��, ��ٻ��, ����. һ����ϳɾۻ�����-�绯ѧ��ԭ����ʯīϩ�������ײ������ڸ����������ù��[J]. �ൺ�Ƽ���ѧѧ��(��Ȼ��ѧ��), 2014, 35(4): 331-335.
LU Zhanguang, KONG Qianqian, YANG Tao. One-step electrosynthesis of ploy(xanthurenic acid)-reduced graphene oxide nanocomposite for highly sensitive detection of chloramphenicol[J]. Journal of Qingdao University of Science and Technology(Natural Science Edition), 2014, 35(4): 331-335.
[6] MOHANTY N, MOORE D, XU Z, et al. Nanotomy-based production of transferable and dispersible graphene nanostructures of controlled shape and size[J]. Nature Communications, 2012, 3: 844.
[7] KIM K S, ZHAO Y, JANG H, et al. Large-scale pattern growth of graphene films for stretchable transparent electrodes[J]. Nature, 2009, 457(7230): 706-710.
[8] WANG X, YOU H, LIU F, et al. Large-scale synthesis of few-layered graphene using CVD[J]. Chemical Vapor Deposition, 2009, 15(3): 53-56.
[9] ������, ���ͱ�, �, ��. ����ʯīϩ�Ŀɿػ�ԭ���ṹ����[J]. �ߵ�ѧУ��ѧѧ��, 2012 (9): 1902-1907.
YANG Xuyu, WANG Xianbao, LI Jing, et al. The controllable reduction and structural characterization of graphene oxide[J]. Chemical Research in Chinese Universities,2012(9):1902-1907.
[10] ����, ����ǿ, �̿�÷, ��. �Ƚⷨ�Ʊ�ʯīϩ�Ĺ��������Ż�[J]. �ൺ�Ƽ���ѧѧ��(��Ȼ��ѧ��), 2013, 34(2): 130-135.
ZHAO Li, LIU Jiaqiang, CHENG Junmei, et al. Processing optimization of graphene prepared by thermal reduction[J]. Journal of Qingdao University of Science and Technology(Natural Science Edition), 2013, 34(2): 130-135.
[11] COLEMAN J N. Liquid-phase exfoliation of nanotubes and graphene[J]. Advanced Functional Materials, 2009, 19(23): 3680-3695.
[12] LIU N, LUO F, WU H, et al. One-step ionic-liquid-assisted electrochemical synthesis of ionic-liquid-functionalized graphene sheets directly from graphite[J]. Advanced Functional Materials, 2008, 18(10): 1518-1525.
[13] CHEN C, LONG M, XIA M, et al. Reduction of graphene oxide by an in-situ photoelectrochemical method in a dye-sensitized solar cell assembly[J]. Nanoscale Research Letters, 2012, 7(1): 1-5.
[14] WILLIAMS G, SEGER B, KAMAT P V. TiO2-graphene nanocomposites UV-assisted photocatalytic reduction of graphene oxide[J]. ACS Nano, 2008, 2(7): 1487-1491.
[15] QIAN H, NEGRI F, WANG C, et al. Fully conjugated tri (perylene bisimides): An approach to the construction of n-type graphene nanoribbons[J]. Journal of the American Chemical Society, 2008, 130(52): 17970-17976.
[16] JIAO L, ZHANG L, WANG X, et al. Narrow graphene nanoribbons from carbon nanotubes[J]. Nature, 2009, 458(7240): 877-880.
[17] ZHU Y, MURALI S, STOLLER M D, et al. Microwave assisted exfoliation and reduction of graphite oxide for ultracapacitors[J]. Carbon, 2010, 48(7): 2118-2122.
[18] DONG S, YI H, LU H, et al. Investigation of gas storage properties of graphene material prepared by microwave-assisted reduction of graphene oxide[J]. Acta Chimica Sinica, 2014, 72(3): 382-387.
[19] COTE L J, CRUZ-SILVA R, HUANG J. Flash reduction and patterning of graphite oxide and its polymer composite[J]. Journal of the American Chemical Society, 2009, 131(31): 11027-11032.
[20] ZHANG Y L, CHEN Q D, XIA H, et al. Designable 3D nanofabrication by femtosecond laser direct writing[J]. Nano Today, 2010, 5(5): 435-448.
[21] BAI H, XU Y, ZHAO L, et al. Non-covalent functionalization of graphene sheets by sulfonated polyaniline[J]. Chemical Communications, 2009(13): 1667-1669.
[22] TUNG V C, ALLEN M J, YANG Y, et al. High-throughput solution processing of large-scale graphene[J]. Nature Nanotechnology, 2009, 4(1): 25-29.
[23] STANKOVICH S, DIKIN D A, PINER R D, et al. Synthesis of graphene-based nanosheets via chemical reduction of exfoliated graphite oxide[J]. Carbon, 2007, 45(7): 1558-1565.
[24] ZHANG J, YANG H, SHEN G, et al. Reduction of graphene oxide via L-ascorbic acid[J]. Chemical Communications, 2010, 46(7): 1112-1114.
[25] ZHU C, GUO S, FANG Y, et al. Reducing sugar: New functional molecules for the green synthesis of graphene nanosheets[J]. ACS Nano, 2010, 4(4): 2429-2437.
[26] ����ǿ. ʯīϩ������Ĺԭ�Լ��������Ʊ��Ļ����о�[D].���֣����ִ�ѧ, 2013.
SHAO Ruiqiang. Fundamental Research on Photoreduction of Graphene Oxides and Their Application in Microdevices Fabrication[D]. Jilin: Jilin University,2013.
[27] AKHAVAN O, ABDOLAHAD M, ESFANDIAR A, et al. Photodegradation of graphene oxide sheets by TiO2 nanoparticles after a photocatalytic reduction[J]. The Journal of Physical Chemistry C, 2010, 114(30): 12955-12959.
[28] MATSUMOTO Y, KOINUMA M, KIM S Y, et al. Simple photoreduction of graphene oxide nanosheet under mild conditions[J]. ACS Applied Materials & Interfaces, 2010, 2(12): 3461-3466.
[29] ���»�, ����, ��ͬ��, ��. ʯīϩ��Ĥ���Ʊ��ͽṹ����[J]. ������ѧѧ��, 2011(3): 736-742.
YANG Yonghui, SUN Hongjuan, PENG Tongjiang, et al. Synthesis and structural characterization of graphene-based membranes[J]. Acta Physico Chimica Sinica, 2011(3): 736-742.
[30] CAO S, CHEN C, LIU T, et al. Polymer-assisted UV excitation method to synthesize reduced graphene oxide/��-Bi2Mo3O12 nanoplates with high activity[J]. Journal of Environmental Chemical Engineering,2014,2(4):2103-2110.
[31] �����, ������, ���Ӣ, ��. ʯīϩ��ǿ���������¸��Ե������о�[J]. ����ѧ��, 2012, 61(21): 262-267.
ZHANG Qiuhui, HAN Jinghuan, FENG Guoying, et al. Raman spectrum research on graphene modification under high intensity laser[J]. Acta Physica Sinica,2012,61(21): 262-267.
[32] ���ϼ, �컪, �Ž�. ����������ʯīϩ�ṹ�����е�Ӧ��[J]. ��ѧѧ��, 2014(3): 301-318.
WU Juanxia, XU Hua, ZHANG Jin. The application of Raman spectroscopy in graphene structure characterization[J]. Acta Chimica Sinica,2014(3): 301-318.
[33] WANG P, LIU Z G, CHEN X, et al. UV irradiation synthesis of an Au-graphene nanocomposite with enhanced electrochemical sensing properties[J]. Journal of Materials Chemistry A, 2013, 1(32): 9189-9195.
(���α༭ �� ��)