»ůÓÚĘŻÄ«Ď©Ľ°Ć临şĎÎďµçĽ«µÄµçČÝČĄŔë×ÓĽĽĘőŃĐľż˝řŐąyd20015
·ë°®»˘, ÓÚÔĆ, ËÎÁ¦ęż ÖĐąúżĆѧԺ ÉĎşŁąčËáŃÎŃĐľżËů, ÖĐąúżĆѧԺĚŘÖÖÎŢ»úÍż˛ăÖصăʵŃéĘŇ, ÉĎşŁ200050
ĘŐ¸ĺČŐĆÚŁş2015-05-11;
ĘŐµ˝Đ޸ĸĺČŐĆÚŁş2015-07-06
×÷Ő߼ň˝éŁş·ë°®»˘(1991¨C), ÄĐ, ˶ʿŃĐľżÉú. E-mail: hpufengaihu@163.com
ͨѶ×÷ŐߣşÓÚÔĆ, ŃĐľżÔ±. E-mail: yunyush@mail.sic.ac.cn
ÔÔŘŁşÎŢ»ú˛ÄÁĎѧ±¨2016/
ˇľŐŞŇŞˇżµçČÝČĄŔë×ÓĽĽĘőĘÇŇ»ÖÖ¸ßЧ˝ÚÄܡ˘ÂĚÉ«»·±ŁµÄÍŃŃη˝·¨, ͨąýĘ©ĽÓľ˛µçłˇ, ÇżÖĆŔë×ÓĎňÁ˝˛ŕµçĽ«Ç¨ŇĆ, ĘąĆä±»µçĽ«±íĂć˛úÉúµÄË«µç˛ăÎü¸˝, ´Ó¶ř´ďµ˝ÍŃŃεÄÄżµÄˇŁµçČÝČĄŔë×ÓĽĽĘőµÄąŘĽüĘǸßĐÔÄܵ缫˛ÄÁϵÄÖƱ¸, ŇŞÇóľßÓнϸߵıȱíĂć»ýˇ˘şĎŔíµÄż×ľ¶·Ö˛ĽşÍÁĽşĂµÄµĽµçĐÔˇŁĘŻÄ«Ď©ľßÓнϸߵÄŔíÂ۱ȱíĂć»ýşÍÓĹŇěµÄµĽµçĐÔ, ĘÇŇ»ÖÖŔíĎëµÄµçĽ«˛ÄÁϡŁČ»¶řÓÉÓÚĘŻÄ«Ď©µÄľŰĽŻĐ§Ó¦, ʵĽĘ±Č±íĂć»ýÔ¶Ô¶µÍÓÚŔíÂŰÖµ, ˝«ĘŻÄ«Ď©ÖƱ¸łÉČýάÍřÂç˝áąą»ň˝«ĘŻÄ«Ď©ÓëĆäËű˛ÄÁĎ˝řĐи´şĎżÉŇԿ˷ţľŰĽŻĐ§Ó¦, Ěá¸ßµçĽ«µÄÍŃŃÎĐÔÄܡŁ±ľÎÄ×ŰĘöÁË»ůÓÚĘŻÄ«Ď©Ľ°Ć临şĎÎďµçĽ«µÄµçČÝČĄŔë×ÓĽĽĘőŃĐľż˝řŐąˇ˘´ćÔÚµÄÎĘĚ⼰ӦÓĂÇ°ľ°ˇŁ
ˇľąŘĽü´ĘˇżĘŻÄ«Ď©; µçĽ«; µçČÝČĄŔë×Ó; ×ŰĘö
ˇľÎÄŐ±ŕşĹˇż1000-324X(2016)02-0123-12DOIŁş10.15541/jim20150231 ÖĐÍĽ·ÖŔŕşĹŁşTB383 ÎÄĎ×±ęʶÂ룺A
Ëć×ĹČËŔŕÉç»áµÄżěËŮ·˘Őą, µË®×ĘÔ´ÎŁ»úłÉÎŞĘŔ˝ç¸÷ąúŘ˝´ý˝âľöµÄÎĘĚâ, Ë®×ĘÔ´¶ĚȱŇŃľłÉÎŞÖĆÔĽ¶ŕąú·˘ŐąµÄÖ÷ŇŞŇňËءŁµŘÇňÉĎ98%µÄË®×ĘÔ´ŇÔşŁË®şÍĎĚË®µÄĐÎĘ˝´ćÔÚ, ˛»ÄÜą©ČËŔŕÖ±˝ÓĘąÓĂ, ·˘ŐąÂĚÉ«¸ßЧµÄşŁË®ÍŃŃÎĽĽĘő˝«ĘÇ˝âľöµË®×ĘÔ´¶ĚȱÎĘĚâµÄÖŘŇŞÍľľ¶[1]ˇŁÄżÇ°, ąă·şĘąÓõĺŁË®µ»ŻĽĽĘőÖ÷ŇŞ°üŔ¨: ·´Éř͸·¨(Reverse osmosis, RO)ˇ˘µçÉřÎö·¨(Electro-dialysis, ED)şÍČČŐô·˘·¨(Thermal evaporation, TE)µČ[2]ˇŁµ«ŐâĐ©ĽĽĘő¶ĽÓĐŇ»¶¨µÄľÖĎŢĐÔ, ĆŐ±é´ćÔÚÄܺĸß, łÉ±ľ¸ßĽ°¶ţ´ÎÎŰČľµČÎĘĚ⡣Čç·´Éř͸ĽĽĘőşÍČČŐô·˘ĽĽĘőĐčŇŞ¸ßÇý¶ŻÄÜÁż, ÄܺĴó, ÍŃŃÎЧÂʵÍ, ÇŇŇײúÉú¶ţ´ÎÎŰČľ[3-4]; ¶řµçÉřÎöĽĽĘőÔňĐč˝Ď¸ßµÄą¤×÷µçŃą[5]ˇŁŇň´Ë, ĆČÇĐĐčŇŞŃĐ·˘µÍłÉ±ľˇ˘¸ßЧÂʺͻ·ľłÓѺõÄĐÂĐÍÂĚÉ«ÍŃŃÎĽĽĘőˇŁ
µçČÝČĄŔë×ÓĽĽĘő(Capacitive deionization, CDI)ľßÓĐą¤×÷µçŃąµÍˇ˘łÉ±ľµÍÇŇÎ޶ţ´ÎÎŰČľµČÓŵă, ĘÇŇ»ÖÖ˝ĎŔíĎëµÄşŁË®µ»Ż·˝·¨, ĆäŔúĘ·żÉŇÔ×·Ëݵ˝20ĘŔĽÍ60Äę´ú, CaudleµČ[6]ĘąÓöŕż×ĚżµçĽ«µÄÁ÷¶ŻµçČÝ×°ÖĂ(Flow-through capacitor)´ÓĽîĐÔË®ÖĐłýČĄŃη֡ŁËćşó, JohnaonµČ[7]ŃĐľżÁ˲»Í¬µÄµçĽ«˛ÄÁĎ, ֤ʵŔë×ÓÔÚ¶ŕż×ĚĽµçĽ«ÉϵÄѡÔńĐÔÎü¸˝, ˛˘Í¨ąý˝řŇ»˛˝µÄŔíÂŰŃĐľż, ĚáłöÁËË«µç˛ăÎü¸˝Ŕë×ӵĸĹÄȻ¶řÖ±µ˝90Äę´úÖĐĆÚ, ĂŔąúŔÍÂ×ËąąúĽŇʵŃéĘҵÄFarmerµČ[8-9]ÖƱ¸łöĚĽĆřÄý˝şµçĽ«şó, ČËĂDzŸüĽÓąŘעCDIĽĽĘőˇŁÖ®şó, Ëćן÷ÖÖ¶ŕż×µçĽ«˛ÄÁϵÄÖƱ¸, CDIĽĽĘőµĂµ˝ÁËżěËŮ·˘ŐąˇŁ
Ň»°ăŔ´Ëµ, CDIµçĽ«˛ÄÁĎŇŞÇóľßÓнϸߵıȱíĂć»ýˇ˘şĎŔíµÄż×ľ¶·Ö˛ĽşÍÁĽşĂµÄµĽµçĐÔ[10]ˇŁ¸ßµÄ±Č±íĂć»ýşÍşĎŔíµÄż×ľ¶·Ö˛ĽżÉŇÔĚáą©¸ü¶ŕµÄżŐλÓĂÓÚÎü¸˝Ŕë×Ó, ÁĽşĂµÄµĽµçĐÔÓĐŔűÓÚĚá¸ßŔë×ӵĴ«ĘäËŮÂĘ, Ěá¸ßµçĽ«µÄ±ČµçČݡŁ¶ŕż×ĚĽ˛ÄÁĎľůÄÜÂú×ăCDIµçĽ«µÄÉĎĘöĚőĽţ, ĘÇŇ»ÖÖŔíĎëµÄCDIµçĽ«˛ÄÁϡŁÄżÇ°ŃĐľż±¨µŔµÄĚĽµçĽ«˛ÄÁĎÖ÷ŇŞ°üŔ¨: »îĐÔĚż[11-12]ˇ˘ĚĽĆřÄý˝ş[10,13]ˇ˘˝éż×ĚĽ[14-15]ˇ˘ĚĽÄÉĂ׹Ü[16-18]şÍĘŻÄ«Ď©[19-21]ˇŁĆäÖĐ, ĘŻÄ«Ď©ĘÇŇ»ÖÖÓÉĚĽÔ×ÓŇÔsp2ÔÓ»ŻąěµŔ×éłÉµÄÁů˝Ç·äł˛ĐÍĆ˝Ă污Ĥ, Ćä±Č±íĂć»ý(2600 m2/g)şÍµçµĽÂĘ(7200 S/m)Ô¶¸ßÓÚ»îĐÔĚżµČĆäËűĚĽ˛ÄÁĎ[22]ˇŁŇň´Ë, ÔÚÄÜÁż´˘´ćĆ÷Ľţ, Č糬Ľ¶µçČÝĆ÷şÍď®Ŕë×ÓµçłŘÖĐÓĐąă·şµÄÓ¦ÓĂ, »ůÓÚʯīϡµçĽ«µÄł¬Ľ¶µçČÝĆ÷µÄČÝÁżżÉ´ďµ˝200 F/gŇÔÉĎ[23]ˇŁ´óÁżŃĐľż±íĂ÷ĘŻÄ«Ď©ÔÚCDIĽĽĘőÖĐ´ćÔÚמ޴óÓ¦ÓĂDZÁ¦, ±ľÎÄ˝«Ďęϸ×ŰĘöʯīϡĽ°Ć临şĎÎď×÷ÎŞCDIµçĽ«µÄŃĐľżĎÖ×´ˇ˘´ćÔÚÎĘĚ⼰ӦÓĂÇ°ľ°ˇŁ
1 ĘŻÄ«Ď©CDIµçĽ«µÄŃĐľż
1.1 ¶ţάʯīϩCDIµçĽ«µÄŃĐľż
ĘŻÄ«Ď©ľßÓнϴóµÄ±Č±íĂć»ýşÍÁĽşĂµÄµĽµçĐÔ, ĘÇŇ»ÖÖŔíĎëµÄCDIµçĽ«˛ÄÁϡŁ2009Äę, »Ş¶«Ę¦·¶´óѧLiµČ[21]ŔűÓøĽřµÄHummer·¨[24-25]şĎłÉÁËŃő»ŻĘŻÄ«, ŇÔË®şĎëÂÎŞ»ąÔĽÁ, ÖƱ¸łöĘŻÄ«Ď©±ˇ˛ă, ˛˘Ę״ν«ĆäÓ¦ÓĂÓÚCDIµçĽ«ˇŁËűĂÇŇÔNaClÎŞČÜŇş, ¶Ô¸ĂµçĽ«˛ÄÁϵÄŔë×ÓÎü¸˝ÄÜÁ¦˝řĐĐÁËŃĐľż, ·˘Ďֵ缫µÄµçÎü¸˝Áż´ďµ˝1.85 mg/g, łő˛˝Ö¤ĘµĘŻÄ«Ď©żÉŇÔ×÷ÎŞCDIµçĽ«˛ÄÁϡŁČ»¶řÖƱ¸µÄĘŻÄ«Ď©±ˇ˛ăµÄ±Č±íĂć»ý˝öÎŞ14.2 m2/g, Ô¶µÍÓÚŔíÂŰÖµ, ËćşóLiµČ[17]ͨąý¸Ä±äʵŃé˛ÎĘýÖƱ¸łö±Č±íĂć»ýÎŞ77 m2/gµÄĘŻÄ«Ď©, ˵Ă÷ĘŻÄ«Ď©µÄ±Č±íĂć»ýÓëÖƱ¸·˝·¨ÓйءŁ
ÄĎ°Ä´óѧZouµČ[26]ŃĐľżÁËHummer·¨ÖĐĎőËáşÍÁňËáµÄş¬Áż¶ÔĘŻÄ«Ď©±ˇ˛ă±Č±íĂć»ýµÄÓ°Ď졣ŃĐľż·˘ĎÖ, µ±Á˝ŐßĚĺ»ý±ČÎŞ1:1ʱ, ÖƱ¸µÄĘŻÄ«Ď©±Č±íĂć»ý×î´ó, ÎŞ222.1 m2/gˇŁµ«˛âĘÔ·˘ĎÖ, »ůÓÚ´ËÖÖĘŻÄ«Ď©µÄCDIµçĽ«µÄµçÎü¸˝Áż˝öÎŞ23.18 ¦Ěmol/g (1.35 mg/g), µÍÓÚ1.85 mg/gˇŁËµĂ÷µçĽ«µÄµçÎü¸˝ĐÔÄܲ»ÍęČ«ÓɲÄÁϵıȱíĂć»ýľö¶¨, ±Č±íĂć»ý˝ö˝öĘÇľö¶¨µçÎü¸˝ĐÔÄܵÄŇ»¸öŇňËءŁ
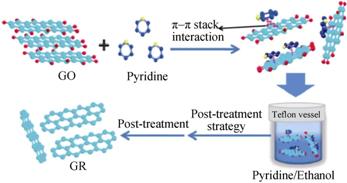
ŔűÓĂŃő»Ż»ąÔ·¨ÖƱ¸ĘŻÄ«Ď©Ę±, »ąÔĽÁµÄѡÔńĘ®·ÖÖŘŇŞˇŁÉĎĘö·˝·¨ÖĐËůÓõ˝µÄ»ąÔĽÁË®şĎëÂÓжľ, ¶řÇŇżÉÄÜ»áÎŰȾʯīϩˇŁÉĎşŁ´óѧZhangµČ[27]ŔűÓĂßÁŕ¤×÷ÎŞ˛ĺČëĽÁşÍ·ÖɢĽÁ, ͨąýČČ˝â°ţŔëµÄ·˝·¨ÖƱ¸łö¸ß·ÖɢĐÔĘŻÄ«Ď©±ˇ˛ă, Ćäşń¶ČÎŞ2.2 nm, şĎłÉą¤ŇŐČçÍĽ1ËůĘľˇŁ˛âĘÔ±íĂ÷, »ůÓÚ´ËÖÖĘŻÄ«Ď©µÄCDIµçĽ«ľßÓĐÁĽşĂµÄµç»ŻŃ§ĐÔÄܡŁ
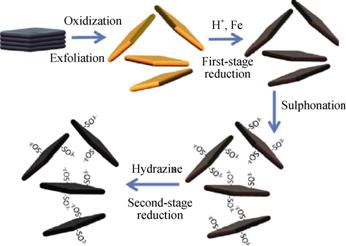
Jia şÍZouµČ[19,28-29]˛ÉÓöಽ»ąÔ·˝·¨, ÓöŕÖÖ»ąÔĽÁ·Ö˛˝»ąÔŃő»ŻĘŻÄ«Ď©, łÉą¦ÖƱ¸łö·ÖɢĐÔ¸üşĂµÄĘŻÄ«Ď©±ˇ˛ă, Ćä±Č±íĂć»ý´ďµ˝464 m2/gˇŁËűĂÇĘ×ĎČĘąÓĂĚú·Ű˝řĐĐłő˛˝»ąÔ, Č»şó˝řĐлǻŻ, ŇýČë![]() , ŇÔ×čֹʯīϩ±ˇ˛ăµÄľŰşĎ[30], ×îşóĘąÓĂË®şĎë½řŇ»˛˝»ąÔ, ÖƱ¸łö·ÖɢĐÔÁĽşĂµÄĘŻÄ«Ď©±ˇ˛ă, ÖƱ¸ą¤ŇŐČçÍĽ2ËůĘľˇŁŃĐľż±íĂ÷, »ůÓÚ´ËÖÖĘŻÄ«Ď©µÄCDIµçĽ«µÄµçÎü¸˝Áż´ďµ˝8.6 mg/g, ±ČµçČÝ´ďµ˝149.8 F/g, µçĽ«ĐÔÄÜÔ¶Ô¶şĂÓÚ֮ǰ±¨µŔˇŁ
, ŇÔ×čֹʯīϩ±ˇ˛ăµÄľŰşĎ[30], ×îşóĘąÓĂË®şĎë½řŇ»˛˝»ąÔ, ÖƱ¸łö·ÖɢĐÔÁĽşĂµÄĘŻÄ«Ď©±ˇ˛ă, ÖƱ¸ą¤ŇŐČçÍĽ2ËůĘľˇŁŃĐľż±íĂ÷, »ůÓÚ´ËÖÖĘŻÄ«Ď©µÄCDIµçĽ«µÄµçÎü¸˝Áż´ďµ˝8.6 mg/g, ±ČµçČÝ´ďµ˝149.8 F/g, µçĽ«ĐÔÄÜÔ¶Ô¶şĂÓÚ֮ǰ±¨µŔˇŁ
|
|
|
ÍĽ1 ßÁनCČȽⷨÖƱ¸ĘŻÄ«Ď©µÄÁ÷łĚÍĽ[27] |
|
|
|
ÍĽ2 ¶ŕ˛˝»ąÔşĎłÉµÄĘŻÄ«Ď©ĘľŇâÍĽ[19] |
×ŰÉĎËůĘö, ˝«ĘŻÄ«Ď©ÓĂÓÚCDIµçĽ«µÄŃĐľżŇѾȡµĂÁËŇ»¶¨µÄłÉĽ¨, ÖƱ¸łöÁ˵çÎü¸˝Áż˝Ď´óµÄĘŻÄ«Ď©µçĽ«˛ÄÁϡŁ˛»Í¬»ąÔ·¨ÖƱ¸µÄĘŻÄ«Ď©µÄµç»ŻŃ§ĐÔÄܲ»Í¬, ѡÔńşĎĘʵÄʵŃéĚőĽţżÉŇԵõ˝ĐÔÄÜÓĹŇěµÄĘŻÄ«Ď©µçĽ«˛ÄÁϡŁµ«ÄżÇ°ÖƱ¸ĘŻÄ«Ď©µÄ·˝·¨Ö÷ŇŞÎŞŃő»Ż»ąÔ·¨, ĘŻÄ«Ď©ÔÚŃő»Ż»ąÔąýłĚÖĐÍůÍů´ćÔÚ·´Ó¦˛»ÍęČ«şÍ¶ţάʯīϩľŰĽŻÎĘĚâ, ŃĎÖŘÓ°ĎěŔë×ӵĴ«ĘäËŮÂʺ͵缫µÄµĽµçĐÔˇŁ´ËÍâ, ľŰĽŻĐ§Ó¦˝µµÍĘŻÄ«Ď©µÄ±Č±íĂć»ý, ˝ř¶řÓ°ĎěµçĽ«µÄµç»ŻŃ§ĐÔÄÜ[31-32]ˇŁ
1.2 ČýάʯīϩCDIµçĽ«µÄŃĐľż
Óë¶ţάʯīϩÄÉĂײÄÁĎĎŕ±Č, Čýάʯīϩ˛ÄÁϵÄ×éÖŻ˝áąą¸üĚŘĘâ, ľßÓиü´óµÄ±Č±íĂć»ýşÍ·Ö˛ĽľůÔȵĿ׾¶, ¸üĘĘşĎ×÷ÎŞCDIµçĽ«˛ÄÁĎ[33-34]ˇŁWangµČ[35]ŔűÓĂWorsley±¨µŔµÄČÜ˝ş¨CÄý˝ş·¨[36]łÉą¦ÖƱ¸łöČýάʯīϩĆřÄý˝ş(RGO-RF), ˛˘˝«ĆäÓ¦ÓĂÓÚCDIµçĽ«ˇŁN2ÎüÍѸ˝µČÎÂĎß±íĂ÷RGO-RFµÄ±Č±íĂć»ýÎŞ406.4 m2/g, Ľ¸şőĘÇÔ¶ţάʯīϩ(RGO)µÄČý±¶Ł¬¶řĆ˝ľůż×ľ¶ÓÉ6.502 nmĽőСµ˝3.124 nm, ¸üÓĐŔűÓÚÎü¸˝NaClŔë×ÓˇŁµçĽ«Îü¸˝ĐÔÄܲâĘÔ±íĂ÷, »ůÓÚRGO-RFµÄCDIµçĽ«µÄµçÎü¸˝ÁżşÍ±ČµçČÝ·Ö±đÎŞ1.424 mg/gşÍ135.7 F/g(ɨĂčËٶČÎŞ10 mV /s), ¸ßÓÚRGOµÄ0.799 mg/gşÍ112 F/g, ±íĂ÷ĘŻÄ«Ď©ĆřÄý˝şľßÓиüşĂµÄµçĽ«ĐÔÄܡŁ´ËÍâ, ËűĂÇ»ą˝řĐĐÁËÎü¸˝¶ŻÁ¦Ń§ŃĐľż, ·˘ĎÖŔë×ÓµÄÎü¸˝Ö÷ŇŞÎŞµĄ˛ăÎü¸˝, Âú×ăŔĘçѶűÎü¸˝µČÎÂÇúĎß, Ŕë×Ó±ĄşÍÎü¸˝ÁżÎŞ13.245 mg/gˇŁ
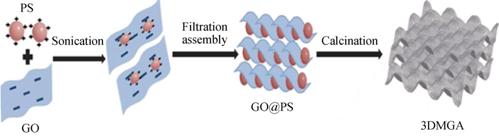
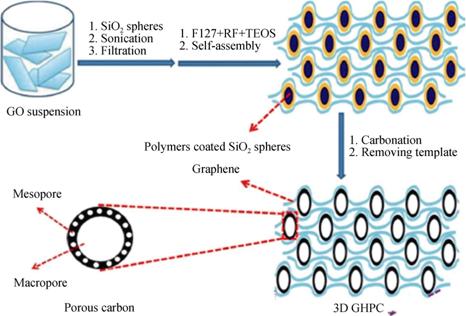
ZhangµČ[37-38]·Ö±đŇԾ۱˝ŇŇĎ©Çň(PS)şÍSiO2Çň×÷ÎŞąÇĽÜ˛ÄÁĎÓëŃő»ŻĘŻÄ«Ë®ČÜŇşľůÔČ»ěşĎ, ľ¸ßÎÂěŃÉŐ, Ńő»ŻĘŻÄ«ČČ˝â°ţŔëÎŞČýά״ʯīϩ, ˛ż·Ö¸ß·Ö×ӾۺĎÎďĚż»ŻĐγɶŕż×ĚĽ, łÉą¦ÖƱ¸łöČýά¶ŕż×ĘŻÄ«Ď©(3DMGA)şÍĘŻÄ«Ď©»ůČýά·ÖĽ¶¶ŕż×ĚĽ˛ÄÁĎ(3DGHPC), şĎłÉąýłĚČçÍĽ3şÍÍĽ4ËůĘľˇŁ
|
|
|
ÍĽ3 3DMGAµÄşĎłÉ·ĎßĘľŇâÍĽ[37] |
|
|
|
ÍĽ4 3DGHPCµÄşĎłÉ·ĎßĘľŇâÍĽ[38] |
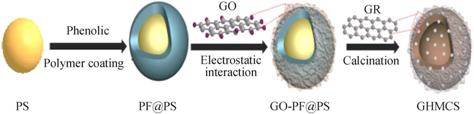
3DMGAşÍ3DGHPCµÄ±Č±íĂć»ý·Ö±đÎŞ339 m2/gşÍ384.4 m2/g, ¸ßÓÚ֮ǰ±¨µŔµÄ¶ţάʯīϩ±ˇ˛ă; µçÎü¸˝ĐÔÄܲâĘÔ±íĂ÷»ůÓÚŐâÁ˝ÖÖČýάʯīϩµÄCDIµçĽ«µÄµçÎü¸˝Áż·Ö±đÎŞ3.9 mg/gşÍ6.18 mg/gˇŁËµĂ÷Čýάʯīϩ¸üĘĘşĎ×÷CDIµçĽ«˛ÄÁϡŁÖ®şó, ËűĂÇÓÖŔűÓĂPSÇňşÍ·ÓČ©Ę÷Ö¬(PF)µČ×÷ÎŞąÇĽÜ˛ÄÁĎ, ÖƱ¸łöÁËŇ»ŔŕеÄČýά˛ÄÁϡŞĘŻÄ«Ď©°ü¸˛µÄÖĐżŐ˝éÖĘĚĽÇň(GHMCS)[39], şĎłÉ·ĎßČç5ÍĽËůĘľ, Ćä±Č±íĂć»ýÎŞ400.4 m2/g, ÔĽÎŞËůÓĂĘŻÄ«Ď©±ˇ˛ăµÄ5±¶ˇŁ
ZhangµČÖƱ¸µÄČýάʯīϩµÄµç»ŻŃ§ĐÔÄÜÓĹŇě, µ«ÖƱ¸ą¤ŇŐ¸´ÔÓ, Çҳɱľ˝Ď¸ß, ˛»ŔűÓÚ´óąćÄŁą¤ŇµÉú˛úˇŁ±±ľ©Ŕíą¤´óѧYangµČ[40]±¨µŔÁËŇ»ÖÖ¸üĽň±ăˇ˘µÍłÉ±ľµÄÖƱ¸·˝·¨, ČçÍĽ6ËůĘľˇŁËűĂÇ˝«Ńő»ŻĘŻÄ«Ď©ČÜŇş˝ţČëµ˝şŁĂŕÖĐ, ľ900ˇćěŃÉŐ, şŁĂŕĎűʧ, Ö±˝ÓµĂµ˝¶ŕż×Čýάʯīϩ˛ÄÁĎ(STGS)ˇŁľ˛âĘÔ, STGSµÄ±Č±íĂć»ýÎŞ305 m 2/g, »ůÓÚSTGSµÄCDIµçĽ«µÄµçÎü¸˝ÁżşÍ±ČµçČÝ·Ö±đÎŞ4.95 mg/gşÍ57 F/g(ɨĂčËٶČÎŞ10 mV /s), ĎŕͬÇéżöĎÂ, ÎŢşŁĂŕąÇĽÜĘŻÄ«Ď©µçĽ«µÄµçÎü¸˝ÁżşÍ±ČµçČÝ˝öÎŞ2.85 mg/gşÍ45 F/gˇŁ´ËÍâ, STGSÖƱ¸µÄµçĽ«ĎÔĘľ¸üşĂµÄŃ»·Îȶ¨ĐÔ, 1000´ÎŃ»·şó, µçĽ«ĐÔÄÜÎȶ¨ÔÚ99%, ÇŇŔë×ÓÍŃÎü¸˝Ę±Ľä˝Ď¶Ě, ˝öÎŞ25 minˇŁ×î˝ü, XuµČ[41]˝«Ńő»ŻĘŻÄ«Ď©ČÜŇşŔ䶳¸ÉÔď, Č»şóÔÚµŞĆřĆř·ŐĎÂ, ľ800ˇćěŃÉŐ3 hÖƱ¸łöÁíŇ»ÖÖşŁĂŕ×´ĘŻÄ«Ď©(GS), ¸ĂGS˛ÄÁϵıȱíĂć»ýÎŞ356.0 m2/g, Ćřż×Ěĺ»ý´ďµ˝1.51 cm3/gˇŁCDIµçĽ«ĐÔÄܲâĘÔ±íĂ÷, ČÜŇşłőʼŨ¶ČÎŞ500 mg/Lʱ, ¸ĂGSµÄµçÎü¸˝ÁżÎŞ14.9 mg/g, ÎŞÔĘŻÄ«Ď©µÄ3.2±¶ˇŁ´ËÍâ, GSµçĽ«µÄ±ČµçČݲâĘÔ˝áąűÎŞ205.2 F/g(ɨĂčËٶČÎŞ5 mV/s), Ô¶¸ßÓÚĆŐͨʯīϩµÄ117.31 F/gˇŁ
|
|
|
ÍĽ5 GHMCSşĎłÉ·ĎßĘľŇâÍĽ[39] |
|
|
|
ÍĽ6 STGS şĎłÉ·ĎßĘľŇâÍĽ[40] |
|
|
|
ÍĽ7 GS şĎłÉ·ĎßĘľŇâÍĽ[41] |
|
|
|
ÍĽ8 KOHĽ¤·˘µÄĘŻÄ«Ď©ŃůĆ·SEMŐŐƬ[46] |
NaOHˇ˘KOHµČÇżĽîżÉÓĂŔ´Ľ¤·˘ĚĽ˛ÄÁĎ, ͨąýżĚĘ´˛ÄÁĎ, ÔöĽÓȱĎÝ, ´Ó¶ř´ďµ˝Ěá¸ßĆä±Č±íĂć»ýşÍµĽµçÂʵÄÄżµÄ[42]ˇŁÄżÇ°¸Ă·˝·¨ŇŃľ±»ąă·şµŘÓ¦ÓĂÓÚCNTs[43]ˇ˘ĚĽĎËά[44]şÍĘŻÄ«Ď©[45]µČĚĽ˛ÄÁϡŁ2015Äę, LiµČ[46]Ę״ν«KOHĽ¤·˘µÄĘŻÄ«Ď©Ó¦ÓĂÓÚCDIĽĽĘő, ÖƱ¸łöş¬´óÁżż×˝áąąµÄČýάʯīϩˇŁ´ÓÍĽ8żÉŇÔż´łöĘŻÄ«Ď©ÎŞČýάÍřÂç˝áąą, ş¬´óÁżż×˝áąąˇŁ˛âĘÔ±íĂ÷, ¸Ă˛ÄÁϵıȱíĂć»ý´ďµ˝3513 m2/g, µĽµçÂĘÎŞ104 S/mˇŁ»ůÓڴ˲ÄÁϵÄCDIµçĽ«µÄµçÎü¸˝Áż´ďµ˝11.86 mg/gˇŁŇÔÉĎĘýľÝłä·Ö±íĂ÷ŔűÓĂĽîĐÔÎďÖĘĽ¤·˘ĘŻÄ«Ď©żÉŇÔÖƱ¸łöĐÔÄÜÓĹŇěµÄCDIµçĽ«˛ÄÁϡŁ
´ÓÉĎĂćµÄÂŰĘöżÉŇÔż´łö, Óë¶ţάʯīϩĎŕ±Č, ČýάʯīϩÄÚ˛żş¬ÓĐ´óÁżµÄąáͨż×˝áąą, Ôö´óÁ˲ÄÁϵıȱíĂć»ýşÍµĽµçĐÔÄÜ, ÖƱ¸łöµÄµçĽ«ľßÓиüşĂµÄŔë×ÓÎü¸˝ĐÔÄÜ, ¸üĘĘşĎ×÷ÎŞCDIµçĽ«˛ÄÁϡŁµ«ÄżÇ°ÖƱ¸ČýάʯīϩµÄą¤Ňսϸ´ÔÓˇ˘łÉ±ľ˝Ď¸ß, ˛»ŔűÓÚą¤Ňµ»ŻÍĆąă, ´ËÍâ, ÖƱ¸µÄČýάʯīϩż×ľ¶˝Ď´ó, ˛»ŔűÓÚÎü¸˝NaClŔë×ÓˇŁ
2 ĘŻÄ«Ď©»ů¸´şĎÎďCDIµçĽ«µÄŃĐľż
˛ă¨C˛ăÖ®ĽäµÄľŰĽŻĐ§Ó¦, µĽÖÂĘŻÄ«Ď©µÄ±Č±íĂć»ýÔ¶µÍÓÚŔíÂŰĽĆËăÖµˇŁŃĐľżŐßĂÇÖ÷ҪͨąýÁ˝ÖÖ·˝·¨˝âľö¸ĂÎĘĚâ[38]: (1)˝«ĘŻÄ«Ď©×öłÉČýάÍřÂç×´, Ôö´ó±Č±íĂć»ý; (2)ŔűÓø÷ÖÖ˛ÄÁĎ×÷ÎŞ˛ĺČëĽÁşÍ·ÖɢĽÁ, Čç»îĐÔĚżˇ˘ĚĽÄÉĂ׹ܡ˘ÄÉĂ×˝đĘôżĹÁŁşÍ¸ß·Ö×ӾۺĎÎďµČ, Ôö´óĘŻÄ«Ď©Ľäľŕ, ĽőÉپۼŻĐ§Ó¦, ´ďµ˝Ôö´óĘŻÄ«Ď©±Č±íĂć»ýµÄÄżµÄˇŁĎÂĂ潫ÖصăĚÖÂŰĘŻÄ«Ď©şÍĆäËű˛ÄÁϵĸ´şĎ¶ÔCDIµçĽ«ĐÔÄܵÄÓ°Ď졣
2.1 ĘŻÄ«Ď©Óë¶ŕż×ĚżµÄ¸´şĎ
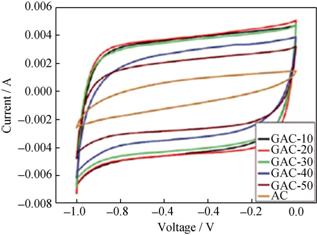
»îĐÔĚż(AC)ľßÓжŕż×˝áąą, Ćä±Č±íĂć»ý¸ß´ď1000 m2/g, ÇŇĽŰÁ®Ň×µĂ, ĘÇCDIłŁÓõĵ缫˛ÄÁĎ, µ«ACż×·Ö˛Ľ˛»ľůÔČ, ŇÔ΢ż×ÎŞÖ÷, ˛»ŔűÓÚÎü¸˝NaClŔë×Ó[10-11,47]ˇŁLiµČ[48]˝«Ńő»Ż»ąÔĘŻÄ«Ď©(RGO)ÓëAC°´˛»Í¬±ČŔý¸´şĎ, ÖƱ¸łö¸´şĎ˛ÄÁĎ(GAC)ˇŁŃĐľż·˘ĎÖ, Ëć×ĹĘŻÄ«Ď©˛ôÁżµÄÔöĽÓ, GACµÄ±Č±íĂć»ýłÖĐřĎ½µ, ͬʱ΢ż×µÄĚĺ»ý»áĽőÉŮ, Ć˝ľůż×ľ¶»áĎČÔö´óşóĽőС, ĆäÖвô20%ĘŻÄ«Ď©µÄGAC-20µÄÖµ×î´ó, ÎŞ2.99 nm, ´ËʱʯīϩµÄ±Č±íĂć»ý´ďµ˝779 m2/gˇŁCVÇúĎßČçÍĽ9ËůĘľ, ĎŕͬĚőĽţĎÂ, »ůÓÚGAC-20µÄµçĽ«µÄ±ČµçČÝ×î´ó, ÎŞ181 F/g, µçÎü¸˝ÁżÎŞ2.94 mg/g, ¸ßÓÚACşÍRGOµÄµçĽ«ˇŁGACÄÚ, RGOşÍACĎ໥˝»ÖŻÔÚŇ»Ćđ, ąąłÉÍřÂç˝áąą, Ň»·˝Ăć¸Ä±äÁËACż×µÄ·Ö˛Ľ, ÁíŇ»·˝ĂćACżĹÁŁĽőÉŮRGOµÄľŰĽŻ×÷ÓĂ, ĽÓÇżRGOÎü¸˝Ŕë×ÓµÄÄÜÁ¦, ´Ó¶řĘąµçĽ«±íĎÖłöÓĹŇěµÄĐÔÄܡŁ
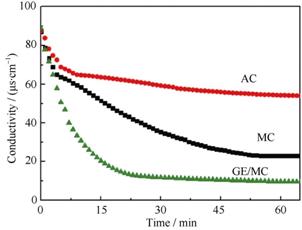
ÓëACĎŕ±Č, ˝éż×ĚĽ(MC)ÓµÓиü´óµÄż×ľ¶, ¸üĘĘşĎÎü¸˝NaClŔë×Ó, ZhangµČ[49]˝«ČČ°ţŔëÖƱ¸µÄĘŻÄ«Ď©(GE)ÓëMC¸´şĎ, ÖƵø´şĎ˛ÄÁĎGE/MCˇŁŃĐľż·˘ĎÖ, ˛ôČëGEżÉÔö´ó˛ÄÁϵıȱíĂć»ý, 5%GE˛ôÔÓÁżµÄGE-5%/MCµÄ±Č±íĂć»ýÎŞ685.2 m2/g, ¸ßÓÚMCµÄ567.7 m2/g, ÇŇż×Ěĺ»ýşÍĆ˝ľůż×ľ¶ľůÓĐÔöĽÓˇŁCDIµçĽ«ĐÔÄܲâĘÔ±íĂ÷, GE/MCµçĽ«±ČµçČÝÔöĽÓ, µ±É¨ĂčËٶČÎŞ1 mV/sʱ, GE-5%/MCµçĽ«ÎŞ89.5 F/g, ¶řMC˝öÎŞ72.55 F/gˇŁ´ËÍâ, GE/MCµçĽ«Ň˛±íĎÖłö¸üşĂµÄŔë×ÓÎü¸˝ĐÔÄÜ, ČçÍĽ10ËůĘľˇŁ
×ŰÉĎËůĘö, ˝«ÉŮÁżĘŻÄ«Ď©Óë¶ŕż×ĚĽ¸´şĎ, ÓÉÓÚĐͬ×÷ÓĂ, ÖƱ¸µÄ¸´şĎ˛ÄÁĎͬʱľß±¸ĘŻÄ«Ď©şÍ¶ŕż×ĚĽµÄĐÔÄÜ, ľßÓĐÁĽşĂµĽµçĐԺͽϴó±Č±íĂć»ýˇŁĘŻÄ«Ď©ÄÚş¬Óп׾¶˝Ď´óµÄƬ˛ă×´ż×, µ±ĘŻÄ«Ď©Óë¶ŕż×ĚĽ¸´şĎʱ, żÉŇÔµ÷˝Ú¶ŕż×ĚĽµÄż×ľ¶·Ö˛Ľ, Ěá¸ßµçĽ«µÄµçÎü¸˝ÄÜÁ¦; ¶ř¶ŕż×ĚĽ×÷ÎŞ˛ĺČëĽÁşÍ·ÖɢĽÁ, ҲżÉÔÚŇ»¶¨łĚ¶ČÉĎ»ş˝âĘŻÄ«Ď©µÄľŰĽŻĐ§Ó¦, ÔöǿʯīϩÎü¸˝Ŕë×ÓµÄÄÜÁ¦, Ęą¸´şĎµçĽ«µÄĐÔÄÜşĂÓÚ´żµÄ¶ŕż×ĚĽşÍĘŻÄ«Ď©µçĽ«ˇŁµ«ÔÚĘŻÄ«Ď©şÍ¶ŕż×ĚĽ¸´şĎąýłĚÖĐ, µ±ĘŻÄ«Ď©ş¬Áż˝ĎÉŮʱ, Ćđ×÷ÓõÄÖ÷ŇŞÎŞ¶ŕż×ĚĽ, µĽÖµ缫µÄµçÎü¸˝Áż˝ĎµÍ; ¶řµ±ĘŻÄ«Ď©µÄş¬Áż˝Ď¸ßʱ,¸´şĎ˛ÄÁϵıȱíĂć»ýÍůÍů»áĎ½µ, Çҵ缫µÄÎȶ¨ĐÔҲ»áĘܵ˝Ó°Ďě[48]ˇŁ
|
|
|
ÍĽ9 NaClÖĐACşÍGACµçĽ«CVÇúĎß(ɨĂčËٶČ1 mV/s)[48] |
|
|
|
ÍĽ10 ACˇ˘MCşÍGE/MCµçĽ«µÄCDIÇúĎ߶ԱČÍĽ[49] |
2.2 ĘŻÄ«Ď©ÓëĚĽÄÉĂ׹ܵĸ´şĎ
ĚĽÄÉĂ׹Ü(CNTs)×÷ÎŞŇ»ÖÖĐÂĐÍÄÉĂײÄÁĎ, ľßÓĐÁĽşĂµÄµĽµçĐÔˇ˘˝Ď´óµÄ±Č±íĂć»ýşÍÁĽşĂµÄ»ŻŃ§¶čĐÔ, һֱ±»ĘÓ×÷ŔíĎëµÄË®´¦ŔíĆ÷ĽţµçĽ«˛ÄÁϵÄŃĐ·˘¶ÔĎó[50-52]ˇŁĘŻÄ«Ď©ÓëĚĽÄÉĂ׹ܸ´şĎʱ, CNTsżÉŇÔ×÷ÎŞ·ÖɢĽÁşÍ˛ĺČëĽÁ, ʹʯīϩ·Öɢ¸üľůÔȡŁÍ¬Ę±, ĘŻÄ«Ď©µÄŇýČëҲżÉŇÔÔöǿ̼ÄÉĂ׹ܵ缫µÄµĽµçĐÔˇŁ
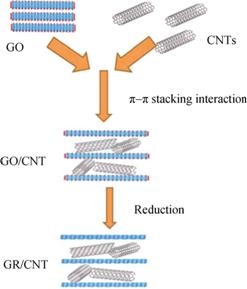
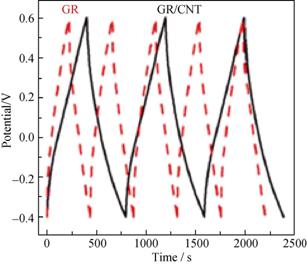
ČçÍĽ11ËůĘľ, CNTsÓëGR¸´şĎʱ, CNTsżÉ˝řČëGR˛ăÖĐ, ʹʯīϩ˝řŇ»˛˝·Öɢ, Ôö´ó±Č±íĂć»ýˇŁZhangµČ[53]˝«˛»Í¬ÁżµÄCNTsĽÓČëµ˝ČČ°ţŔëÖƱ¸µÄGRÖĐ, ÖƱ¸łöÍř×´¸´şĎ˛ÄÁĎ(GR/CNT)ˇŁÓëGRĎŕ±Č, ·˘ĎÖ˛ôCNTsµÄGRµÄ±Č±íĂć»ýşÍĆřż×Ěĺ»ýÔöĽÓˇŁĆäÖĐ, 10%CNTs˛ôÔÓÁżµÄGR/CNT-10%±Č±íĂć»ýÎŞ479.5 m2/g, Ěá¸ßÁË39.8%, Ćřż×Ěĺ»ýÔöĽÓÁË32.9%ˇŁÍ¬Ę±, µçĽ«ĐÔÄܲâĘÔ±íĂ÷, GR/CNT-10%µçĽ«µÄ±ČµçČÝÎŞ68 F/g(ɨĂčËٶČÎŞ10 mV/s), ¸ßÓÚGRµçĽ«µÄ32 F/gˇŁ´ËÍâ, GR/CNT-10%µçĽ«µÄµçÎü¸˝Áż´ďµ˝1.41 mg/g, ¶řGRµçĽ«µÄֵΪ1.10 mg/gˇŁŃ»·ÍŃÎü¸˝ĘµŃéÔň±íĂ÷GR/CNTµçĽ«Îȶ¨ĐÔÄܸüşĂ, ČçÍĽ12ËůĘľˇŁLiµČ[54]˝«ÉŮÁżµÄŃő»Ż»ąÔĘŻÄ«Ď©(RGO)˛ôÔÓµ˝CNTs, ÖƱ¸łöCNTs-RGO, ÓĂŔ´ŃĐľż˛»Í¬ĘŻÄ«Ď©˛ôČëÁż¶ÔCNTsµçĽ«ĐÔÄܵÄÓ°Ď졣ËűĂÇ·˘ĎÖ, 10%˛ôČëÁżµÄCNTs-RGO-10ÖƱ¸µÄµçĽ«˛ÄÁϵÄĐÔÄÜ×îşĂ, Ćä±ČµçČÝÎŞ311.1 F/g(ɨĂčËٶČ10 mV/s), ´óÓÚCNTsµçĽ«µÄ202 F/gşÍRGOµçĽ«µÄ293.4 F/gˇŁŇÔÉĎʵŃéľů˵Ă÷ÁËĘŻÄ«Ď©şÍĚĽÄÉĂ׹ܸ´şĎ, żÉŇÔÖƱ¸łöĐÔÄÜÓĹŇěµÄ¸´şĎµçĽ«˛ÄÁϡŁ
|
|
|
ÍĽ11 GR/CNT şĎłÉĘľŇâÍĽ[53] |
|
|
|
ÍĽ12 GR/CNTşÍGRµçĽ«łä·ĹµçÇúĎß[53] |
WimalasirişÍZou[55-56]µČ°´10:1µÄ±ČŔý˝«Ńő»ŻĘŻÄ«Ď©GOşÍµĄ±ÚĚĽÄÉĂ׹Ü(SWCNTs)»ěşĎ, ŔűÓĂË®şĎë½řĐĐ»ąÔ´¦Ŕí, ÖƱ¸łö¸´şĎ˛ÄÁĎCNT/G, ˛˘˝«ĆäÓ¦ÓĂÓÚCDIµçĽ«ˇŁÖµµĂעŇâµÄĘÇ, CNT/G˛ÄÁϵıȱíĂć»ýÎŞ391 m2/g, Óë֮ǰ±¨µŔµÄĘýľÝŔŕËĆ, µ«µçĽ«µÄµçÎü¸˝Áż´ďµ˝ÁË26.42 mg/g, ±ČµçČÝ´ďµ˝213 F/g(ɨĂčËٶČ10 mV/s), Ô¶´óÓÚ֮ǰ±¨µŔµÄÖµˇŁWimalasirişÍZou˝«Ćäąéą¦ÓÚCNT/G¸´şĎ˛ÄÁĎÖƱ¸ą¤ŇյIJ»Í¬ˇŁ
ĚĽÄÉĂ׹ܿÉŇÔĚá¸ßĘŻÄ«Ď©µÄµĽµçĐÔĽ°±Č±íĂć»ý, ¶ţŐß˝áşĎżÉĐÎłÉÍř×´¸´şĎµçĽ«˛ÄÁϡŁ»ůÓڸø´şĎ˛ÄÁϵÄCDIµçĽ«µÄµçÎü¸˝Áż˝Ď´ó, ±íĎÖłöÓĹŇěµÄµç»ŻŃ§ĐÔÄܡŁŇň´Ë, ˝«ĘŻÄ«Ď©ÓëĚĽÄÉĂ׹ܽřĐи´şĎĘÇŇ»ÖÖĚá¸ßµçĽ«ĐÔÄܵĿÉĐĐÍľľ¶ˇŁ
2.3 ĘŻÄ«Ď©ÓëÄÉĂ×˝đĘôżĹÁŁµÄ¸´şĎ
ÎŞÁ˸ÄÉĆĘŻÄ«Ď©µÄ·ÖɢĐÔ, żÉ˝«¸ßµçČݵÄÄÉĂ×˝đĘôżĹÁŁ×÷ÎŞ·ÖɢÎďĚíĽÓµ˝ĘŻÄ«Ď©˛ăÖĐ, ´Ó¶ř´ďµ˝Ôö´ó±Č±íĂć»ýµÄÄżµÄˇŁ´óÁżŃĐľż±íĂ÷ŇÔĘŻÄ«Ď©şÍÄÉĂ×˝đĘôżĹÁŁµÄ¸´şĎÎď×÷ÎŞµçĽ«˛ÄÁĎ, żÉŇÔĚá¸ßł¬Ľ¶µçČÝĆ÷±ČµçČÝ[57-58], Ҳ´Ó˛ŕĂćÂŰÖ¤ÁËĘŻÄ«Ď©şÍÄÉĂ×˝đĘô¸´şĎÎďÔöÇżCDIµçĽ«ĐÔÄܵĿÉĐĐĐÔˇŁ
¶ţŃő»ŻÎý(SnO2)ĘÇŇ»Öּ۸ńµÍÁ®, »·ľłÓŃşĂĐ͵ÄŃő»ŻÎď˝đĘô, ÇŇľßÓĐÁĽşĂµÄ»ŻŃ§Îȶ¨ĐԺ͸ߵçČÝ, ŇŃľÔÚď®Ŕë×ÓµçłŘµçĽ«şÍ´«¸ĐĆ÷ÁěÓň±íĎÖłöÁËÓĹŇěµÄÓ¦ÓĂÇ°ľ°[59]ˇŁEl-DeenµČ[60]˝«ÄÉĂ×SnO2ÓëĘŻÄ«Ď©¸´şĎ, ˛ÉÓá°Ň»ąřşĎłÉ·¨ˇ±ÖƱ¸łöĐÂĐ͸´şĎCDIµçĽ«˛ÄÁĎGr/SnO2ˇŁľ˛âĘÔ, µ±SnO2˛ôÁżÎŞ15%ʱ, µçĽ«±íĎÖłö×îşĂµÄĐÔÄÜ, Ćä±ČµçČÝÎŞ323 F/g(ɨĂčËٶČ5 mV/s), ÍŃŃÎÂĘ´ďµ˝83%, µçÎü¸˝ÁżÎŞ1.49 mg/gˇŁÖ¤Ă÷ÁËÄÉĂ×˝đĘôżĹÁŁżÉŇÔĽőČőĘŻÄ«Ď©µÄľŰşĎ×÷ÓĂ, Ôö´óĘŻÄ«Ď©±Č±íĂć»ýˇŁĘŻÄ«Ď©Óë˝đĘôżĹÁŁµÄ¸´şĎ, ÎŞĚá¸ßĘŻÄ«Ď©»ůCDIµçĽ«ĐÔÄÜĚáą©ÁËŇ»ÖÖеķ˝·¨ˇŁ
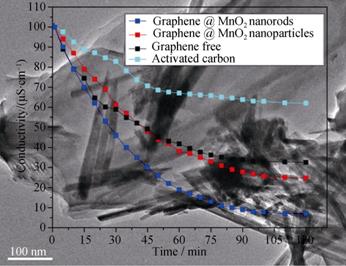
Ö®şó, El-DeenµČ[61]ÓÖŃĐľżÁ˲»Í¬ĐÎ×´µÄÄÉĂ×MnO2¶ÔĘŻÄ«Ď©CDIµçĽ«µÄÓ°Ď졣ËűĂÇ˝«żĹÁŁ×´ÄÉĂ×MnO2(MnO2-NPs)şÍ°ô×´ÄÉĂ×MnO2(MnO2-NRs)·Ö±đÓëĘŻÄ«Ď©¸´şĎ, ÖƱ¸łö¸´şĎµçĽ«˛ÄÁĎMnO2- NPs@GRşÍMnO2-NRs@GRˇŁ¶Ô±Č·˘ĎÖMnO2-NRsĽÓǿʯīϩ·ÖɢłĚ¶ČµÄЧąű¸üĂ÷ĎÔ, CDIµçĽ«±íĎÖłö¸üşĂµÄĐÔÄܡŁMnO2-NRs@GRµçĽ«µÄ±ČµçČÝ´ďµ˝292 F/g, µçÎü¸˝ÁżÎŞ5.01 mg/g, ÍŃŃÎÂĘÎŞ93%ˇŁ´ÓÍĽ13żÉŇÔż´łöGRˇ˘ACŇÔĽ°MnO2-NPs@GRµçĽ«µÄŔë×ÓÎü¸˝ÄÜÁ¦şÍMnO2-NRs@GRµçĽ«µÄ¶Ô±ČˇŁ
|
|
|
ÍĽ13 ˛»Í¬µçĽ«µÄCDIÇúĎ߶ԱČÍĽ[61] |
˝đĘôŇř(Ag)ľßÓĐÁĽşĂµÄČČÎȶ¨ĐÔˇ˘µĽµçĐÔ[62]şÍɱľúą¦ÄÜ[63], ÎŞÁËĚá¸ßCDIµçĽ«µÄµçÎü¸˝ĐÔÄÜşÍɱľúĐÔÄÜ, CaiµČ[64]˝«ÄÉĂ×AgĚíĽÓµ˝ĘŻÄ«Ď©ÖĐ, ÖƱ¸łö¸´şĎCDIµçĽ«˛ÄÁĎAg/rGOˇŁ´ËÍâ, ËűĂÇ»ąÍ¨ąýAg+-¦Â-»·şýľ«(CD)µÄĚż»ŻąýłĚ, ÖƱ¸łöAg@CÄÉĂ׿ĹÁŁ, ˛˘˝«ĆäÓëĘŻÄ«Ď©¸´şĎÖƱ¸łöAg@C/rGOµçĽ«˛ÄÁϡŁµçĽ«ĐÔÄܲâĘÔ±íĂ÷, Ag/rGOşÍAg@C/rGO µçĽ«żÉŇÔĽőÉŮłäµç×čÁ¦, µçÎü¸˝ĐÔÄܸüşĂˇŁÍŃÎü¸˝Ę±, 5 minÄڵ缫żÉŇÔ»Ö¸´µ˝90%ŇÔÉĎ, ÇŇAg/rGO şÍAg@C/rGOµçĽ«żÉŇÔĂ÷ĎÔµŘÔöĽÓżąľúÄÜÁ¦, ĽőÉŮϸľúµÄ×ĚÉúˇŁ
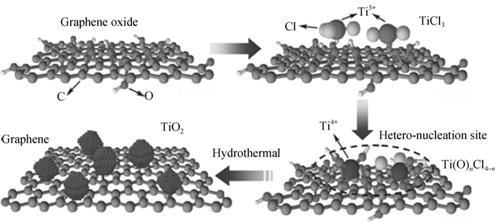
¶ţŃő»ŻîŃ(TiO2)ĘÇŇ»ÖÖÓĹÖʵĽđĘôŃő»ŻÎď, ľßÓеͶľˇ˘¸ßÎȶ¨ĐԺ͸߽éµçłŁĘýµČĐÔÖĘ, ĘÇŇ»ÖÖŔíĎëµÄÔöǿʯīϩµçĽ«ĐÔÄܵĽđĘô˛ÄÁĎ[65]ˇŁYinµČ[66]ŇÔTiCl3şÍGOÎŞÇ°ÇýÎď, PVPÎŞÎȶ¨ĽÁ, ˝«ČýάʯīϩşÍTiO2ÄÉĂ׿ĹÁŁ¸´şĎ, ÖƱ¸łö¸´şĎµçĽ«˛ÄÁĎGA/TiO2, ĆäşĎłÉ·ĎßČçÍĽ14ËůĘľˇŁľ˛âĘÔ, µ±NaClłőʼŨ¶ČÎŞ500 mg/Lʱ, GA/TiO2µçĽ«µÄµçÎü¸˝ÁżÎŞ15.1 mg/g, ·Ö±đĘÇGAµçĽ«µÄ1.5±¶, ACµçĽ«µÄ12.6±¶ˇŁ2015Äę, El-DeenµČ[67]˝«TiO2ÓëĘŻÄ«Ď©¸´şĎÖƱ¸łö¸´şĎ˛ÄÁĎ(rGO/TiO2), ˛˘˝«ĆäÓ¦ÓĂÓÚĤµçČÝČĄŔë×ÓĽĽĘő(MCDI)ÖĐ, ·˘ĎÖ˛ô20%TiO2µÄ¸´şĎµçĽ«µÄ±ČµçČÝ´ďµ˝443 F/g(ɨĂčËٶČ10 mV/s), ÎŞrGOµçĽ«µÄ9±¶ˇŁą¤×÷µçѹΪ0.8 V, łőʼҺŨ¶ČÎŞ300 mg/L, ¸´şĎµçĽ«µÄµçÎü¸˝Áż´ďµ˝9.1 mg/g, ±íĎÖłöÓĹŇěµÄCDIµçĽ«ĐÔÄܡŁ
×ŰÉĎËůĘö, ÄÉĂ×˝đĘô×÷ÎŞ·ÖɢÎďÖĘ, żÉŇԺܺõŘʹʯīϩľůÔČ·Öɢ, ´ďµ˝ÔöÇżCDIµçĽ«ĐÔÄܵÄÄżµÄˇŁ˛»Í¬µÄÄÉĂ×˝đĘô, ˛»Í¬µÄĐÎ×´ľů»áÓ°Ď츴şĎµçĽ«µÄĐÔÄÜ, ĆäÖĐ°ô×´ÄÉĂ׿ĹÁŁ×÷ÓĂЧąű¸üşĂˇŁ˝«ÄÉĂ×˝đĘôÓëČýάʯīϩ¸´şĎ, ÓĐÍűµĂµ˝ĐÔÄܸüĽÓÓĹŇěµÄĘŻÄ«Ď©»ů¸´şĎµçĽ«˛ÄÁϡŁµ«ĘÇŇÔÉĎŃĐľżÎ´żĽÂÇÄÉĂ×˝đĘôżĹÁŁÔÚŃÎČÜŇşÖеÄÎȶ¨ĐԶԵ缫ĐÔÄܵÄÓ°Ďě; ÍŃŃÎąýłĚÖĐ, ÄÉĂ×˝đĘôżĹÁŁżÉÄܲż·ÖČÜ˝âÓÚČÜŇşÖĐ, ÎŰČľČÜŇşˇŁ´ËÍâ, ÄÉĂ×˝đĘôżĹÁŁµÄ´ćÔÚҲżÉÄÜ´Ů˝řË®µÄµç˝â·´Ó¦şÍĘŻÄ«Ď©±íĂćµÄŃő»Ż·´Ó¦µČ, ˝řŇ»˛˝Ó°Ď츴şĎµçĽ«µÄµç»ŻŃ§ĐÔÄÜşÍÎȶ¨ĐÔˇŁ
|
|
|
ÍĽ14 GA/TiO2şĎłÉ·ĎßĘľŇâÍĽ[66] |
2.4 ĘŻÄ«Ď©ÓëľŰşĎÎďµÄ¸´şĎ
һЩĚŘĘâµÄµĽµç¸ß·Ö×ӾۺĎÎď, ČçľŰ±˝°·(PANI), ŇňĆäľßÓиߵĽµçĐÔşÍŇ׺ϳÉĐÔ[68-70], łÉÎŞŃĐľżČȵ㡣˝«µĽµçľŰşĎÎďÓë¶ŕż×ĚĽ˛ÄÁϸ´şĎĘÇÖƱ¸¸´şĎµçĽ«˛ÄÁϵÄÖŘŇŞ·˝·¨, ÖƱ¸µÄ¸´şĎµçĽ«µÄµç»ŻŃ§ĐÔÄܸüĽŃ, µ«ÄżÇ°¸Ă¸´şĎµçĽ«Ö÷ŇŞĘÇÓ¦ÓĂÓÚď®Ŕë×ÓµçłŘşÍł¬Ľ¶µçČÝĆ÷µČˇŁ
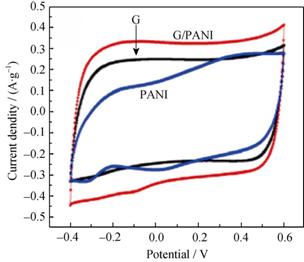
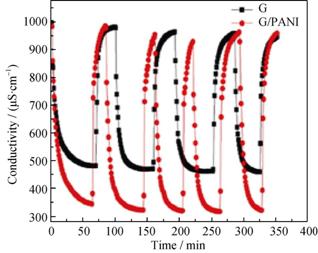
YanµČ[71]˝«ĘŻÄ«Ď©ÓëPANI¸´şĎ, ͨąýÔλľŰşĎ·¨ÖƱ¸łö¸´şĎµçĽ«˛ÄÁĎG/PANIˇŁËűĂÇ˝«ĘŻÄ«Ď©ÓëPANIµĄĚĺ±˝°·»ěşĎ, ±˝°·ÔÚąýÁňËáď§×÷ÓĂĎÂ, ľľŰşĎ×÷ÓúϳÉPANI, şĎłÉµÄPANIÓëĘŻÄ«Ď©Ďŕ˝áşĎ, ĐÎłÉG/PANI¸´şĎ˛ÄÁĎ, şĎłÉ·ĎßČçÍĽ15ËůĘľˇŁN2Îü¸˝˛âĘÔ±íĂ÷G/PANI±Č±íĂć»ýÎŞ394 m2/g, µÍÓÚĘŻÄ«Ď©µÄ428 m2/g, µ«G/PANIµÄż×ľ¶·Ö˛ĽÔÚ2~6 nm, ¸üĘĘşĎÎü¸˝Ŕë×Ó[52]ˇŁ´ÓÍĽ16żÉż´łöG/PANIµçĽ«µÄµç»ŻŃ§ĐÔÄܸüĽŃ, ±ČµçČݸü´ó, ÍĽ17Ôň±íĂ÷ÁËG/PANIµçĽ«µÄŃ»·ÔŮÉúĐÔÄܡŁÓÉ´Ë˵Ă÷G/PANIµçĽ«ľßÓиüşĂµÄµçĽ«ĐÔÄÜ, ĘŻÄ«Ď©ÓëľŰşĎÎďPANI¸´şĎżÉŇÔÖƱ¸łöĐÔÄÜÓĹŇěµÄµçĽ«˛ÄÁϡŁ
Ŀǰ, ĘŻÄ«Ď©ÓëľŰşĎÎ︴şĎÓĂÓÚCDIµçĽ«µÄ±¨µŔ˝ĎÉ١Łµ«´ÓĆäÔÚł¬Ľ¶µçČÝÖеÄÓ¦ÓĂ[69,72]şÍYanµČ[71]µÄŃĐľżżÉŇÔż´łö, µĽµçĐԾۺĎÎďżÉŇÔÔöÇż¸´şĎµçĽ«µÄµĽµçĐÔ, ĽÓżěŔë×ÓĘäÔËËŮÂĘ, Ěá¸ßµçĽ«±ČµçČÝşÍŔë×ÓÍŃÎü¸˝ËŮÂʡŁµĽµçľŰşĎÎď×÷ÎŞ·ÖɢĽÁşÍ˛ĺČëĽÁ, żÉŇÔÔö´óĘŻÄ«Ď©˛ăĽäľŕ, Ôö´óĆä±Č±íĂć»ý, µ«ĘǵĽµç¸ß·Ö×ÓҲżÉÄÜ»áʹʯīϩÄÚ˛ż·ÖĆřż×¶ÂČű, Ęą´˘´ćŔë×ӵĿŐλĽőÉ١Ł´ËÍâ, µ±µĽµç¸ßľŰÎďŨ¶Čąý¸ßʱ, Ćä·Öɢ˛»ľůÔČ, żÉÄÜ»áĐÎłÉÍĹľŰĚĺ, Ó°ĎěµçĽ«µÄµĽµçĐÔˇŁ
2.5 ĘŻÄ«Ď©ÓëĚĽĎËάµÄ¸´şĎ
ŔűÓĂľ˛µç·ÄËżĽĽĘő, żÉŇÔÖƱ¸łö±Č±íĂć»ý´óˇ˘µĽµçĐÔÄÜÁĽşĂµÄ¶ŕż×ÄÉĂ×ĚĽĎËάÍř, ˝«ĆäÓĂÓÚCDIµçĽ«˛ÄÁĎ, ŇŃľ±íĎÖłöÓĹŇěµÄµçĽ«ĐÔÄÜ[73-74]ˇŁĘŻÄ«Ď©ľßÓн϶ŕµÄÖп׺ÍÓĹŇěµÄµĽµçĐÔÄÜ, ÓëĚĽĎËά¸´şĎ, żÉŇÔµ÷˝Ú˛ÄÁϿ׾¶·Ö˛Ľ, ÖƱ¸łöĐÔÄܸüĽÓÓĹŇěµÄCDIµçĽ«˛ÄÁϡŁ
|
|
|
ÍĽ15 ÔλľŰşĎ·¨ÖƱ¸PANI şÍĘŻÄ«Ď©¸´şĎÎď[71] |
|
|
|
ÍĽ16 Gˇ˘PANIşÍG/PANIµçĽ«µÄCVÇúĎß[71] |
|
|
|
ÍĽ17 µçĽ«µÄÍŃÎü¸˝ÇúĎß[71] |
2013Äę, Ç廪´óѧBaiµČ[75]ŔűÓĂľ˛µç·ÄËżĽĽĘő, ÖƱ¸łö˛ôÉŮÁżĘŻÄ«µÄ¶ŕż×ĚĽĎËάGO-PCNFşÍÎŢĘŻÄ«Ď©µÄPCNFÍř×´˛ÄÁϡŁŃĐľż·˘ĎÖ, ĘŻÄ«Ď©µÄŇýČëĘą˛ÄÁϵıȱíĂć»ýĽőСÁË18.7%, µ«Öп׵ıČÂĘÔöĽÓÁË18%, ¸üÓĐŔűÓÚNaClŔë×ÓµÄÎü¸˝ˇŁµçĽ«ĐÔÄܲâĘÔ·˘ĎÖ, GO-PCNFşÍPCNFµçĽ«ľůľßÓнϸߵÄŔë×ÓÎü¸˝ÄÜÁ¦ˇŁµ±łőʼŨ¶ČÎŞ100 mg/Lʱ, GO-PCNFµçĽ«µÄµçÎü¸˝ÁżÎŞ7.8 mg/g, PCNFµçĽ«ÎŞ5.9 mg/g, ËůŇÔGO-PCNFµçĽ«µÄŔë×ÓÎü¸˝ĐÔÄÜ»á¸üşĂһЩˇŁµçĽ«µÄ±ČµçČݲâĘÔҲ±íĂ÷GO-PCNFµçĽ«µÄÖµ˝Ď¸ß, ÎŞ156.1 F/gˇŁ
Dong µČ[76]ŔűÓĂľ˛µç·ÄËżĽĽĘő˝«˛»Í¬ÁżµÄŃő»Ż»ąÔĘŻÄ«Ď©(RGO)Óë»îĐÔĚĽĎËά(ACF)¸´şĎ, ÖƱ¸łöRGO/ACFÍř×´¸´şĎÎŃĐľż·˘ĎÖ, RGOµÄ˛ôČëżÉŇÔ¸ÄÉƿ׾¶·Ö˛Ľ, ÔöÇżµçĽ«ĐÔÄܡŁĆäÖвô10%RGOµÄRGO/ACF-10µçĽ«ĎÔĘľłöÁË×îĽŃµÄŔë×ÓÎü¸˝ÄÜÁ¦, µçÎü¸˝ÁżÎŞ7.2 mg/g, ±ČACFµçĽ«¸ß53%ˇŁ
×ŰÉĎËůĘö, ŔűÓĂľ˛µç·ÄËżĽĽĘő, ˝«ĘŻÄ«Ď©ÓëÄÉĂ×ĚĽĎËά¸´şĎ, żÉŇÔÖƱ¸łöĐÔÄÜÓĹŇěµÄCDIµçĽ«˛ÄÁϡŁŐâĘÇÓÉÓÚĘŻÄ«Ď©µÄŇýČë, ¸ÄÉĆÁ˲ÄÁϵĿ׾¶·Ö˛Ľ, Ôö´óÁËÖп׵ıČÂʡŁµ«ĘÇĿǰµÄŃĐľżÖĐĘŻÄ«Ď©µÄ˛ôČëÁż˝ĎµÍ, δÄÜłä·Ö·˘»ÓĘŻÄ«Ď©ÓĹŇěµÄĐÔÄÜ, CDIµçĽ«ĐÔÄÜ»ąÓĐ´ýĚá¸ßˇŁ
|
±í1 ˛»Í¬ĘŻÄ«Ď©»ůµçĽ«˛ÄÁϵÄĐÔÄÜ¶Ô±Č |
|
|
3 ×Ü˝á
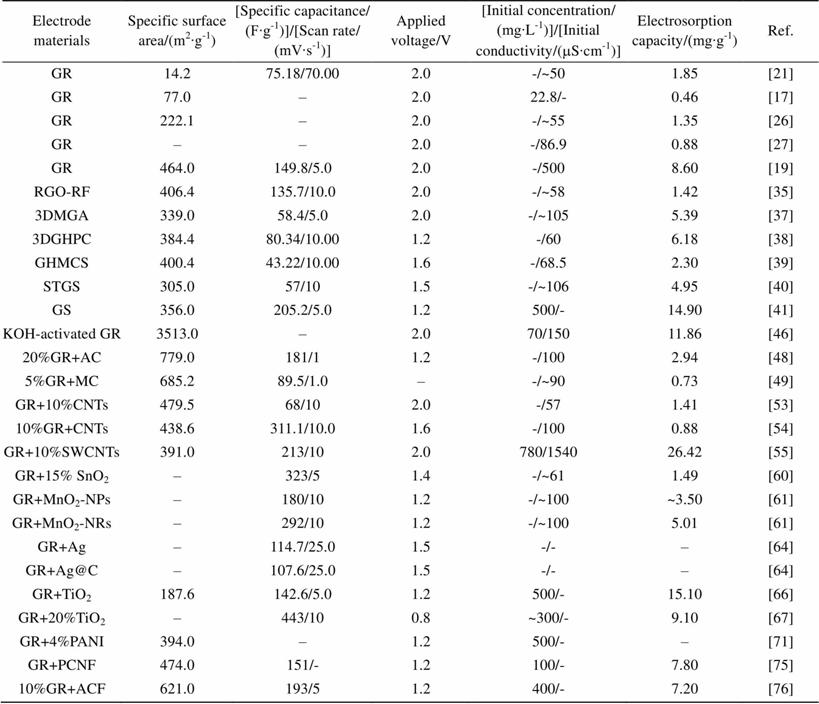
ÓÉÓÚĘŻÄ«Ď©µÄľŰĽŻĐ§Ó¦, µĽÖ±ȱíĂć»ý˝öÎŞ~80 m2/g, Ô¶µÍÓÚŔíÂŰÖµ, ąĘ¶ţάʯīϩ±ˇ˛ăCDIµçĽ«Đ§ąű˛˘˛»şĂ, ČýάʯīϩľßÓжŔĚصĹáͨż×˝áąą, żÉŇÔÔö´ó±Č±íĂć»ý, ¸ÄÉƵ缫ĐÔÄܡŁĘŻÄ«Ď©ÓëACˇ˘MCˇ˘CNFsşÍĚĽÄÉĂ×ĎËάµČ¸´şĎżÉĎÔÖř¸ÄÉƿ׾¶µÄ·Ö˛Ľ, Ěá¸ßµçĽ«µÄµçÎü¸˝ĐÔÄܡŁÄżÇ°, ĘŻÄ«Ď©Ľ°Ć临şĎÎďÔÚCDIşŁË®µ»ŻÁěÓňÖĐŇѾȡµĂÁËŇ»¶¨µÄ˝řŐą, ¸÷ÖÖĘŻÄ«Ď©»ůCDIµçĽ«ĐÔÄܶԱČČç±í1ËůĘľˇŁµ«ÄżÇ°µÄŃĐľżČÔ´¦ÓÚłőĘĽ˝×¶Î, ČÔ´ćÔÚһЩĐčĽĚĐřÉîČëŃĐľżµÄÎĘĚ⡣
1) ÖƱ¸µÄĘŻÄ«Ď©˛ÄÁĎÖĘÁż˛»Îȶ¨ˇŁÎÄÖĐËůÉ漰µÄ´ó¶ŕÎŞŃő»Ż»ąÔĘŻÄ«Ď©, ĆäÖƱ¸ąýłĚÖв»Č·¶¨ĐÔŇňËغܶࡣĎŕͬĚőĽţÖƱ¸µÄĘŻÄ«Ď©±Č±íĂć»ýˇ˘ż×ľ¶·Ö˛ĽµČ˛î±đ˝Ď´ó, µĽÖÂÖƱ¸µÄµçĽ«ĐÔÄܲ»Îȶ¨, ˛»ŔűÓÚą¤Ňµ»ŻÍƹ㡣
2) CDIµçĽ«µÄÎȶ¨ĐÔŘ˝´ý˝âľöˇŁĐč×ۺϿĽÂÇÓ°ĎěCDIµçĽ«µÄŇňËŘ, ˛ż·ÖŃĐľż˝ö˝ö˛âĘÔÁ˵缫µÄĽ¸¸öŃ»·ÍŃÎü¸˝ÇúĎß, ±ăµĂłöµçĽ«Ę®·ÖÎȶ¨µÄ˝áÂŰ, Č»¶ř˛˘ÎŢ·¨±ŁÖ¤CDIµçĽ«µÄł¤ĆÚÎȶ¨ĐÔˇŁ
3) δżĽÂÇʵĽĘşŁË®»·ľł¶ÔCDIµçĽ«µÄÓ°Ď졣Ŀǰ˝öŔűÓĂNaClČÜŇş˝řĐĐĎŕąŘŃĐľż, δżĽÂǸ´ÔÓşŁË®×é·Ö¶ÔCDIµçĽ«Ó°Ď졣
ËäȻĿǰ´ćÔÚĐí¶ŕĽĽĘőĚôŐ˝, µ«CDIĽĽĘő×÷ÎŞŇ»ÖÖ¸ßЧ˝ÚÄܡ˘ÂĚÉ«»·±ŁµÄÍŃŃÎą¤ŇŐ, ČÔČ»ĎÔĘľłöľŢ´óµÄÓ¦ÓĂÇ°ľ°, ˛»˝öżÉŇÔÓ¦ÓĂÓÚşŁË®µ»Ż, »ążÉÓ¦ÓĂÓÚÖŘ˝đĘôÝÍȡˇ˘ÎŰË®ÍŃŃδ¦ŔíµČÁěÓňˇŁ´ËÍâ, CDIĽĽĘőżÉŇÔͨąýѡȡşĎĘʸ´şĎµçĽ«˛ÄÁĎ, ʵĎÖѡÔńĐÔłýČĄÄż±ęŔë×ÓµÄÄżµÄ, Ó¦ÓĂÓÚË®Čí»ŻµČÁěÓňˇŁ
˛ÎżĽÎÄĎףş
[1] SHANNON M A, BOHN P W, ELIMELECH M, et al. Science and technology for water purification in the coming decades. Nature, 2008, 452(7185): 301¨C310.
[2] ANDERSON M A, CUDERO A L, PALMA J. Capacitive deionization as an electrochemical means of saving energy and delivering clean water. Comparison to present desalination practices: will it compete? Electrochimica Acta, 2010, 55(12): 3845¨C3856.
[3] ZOU L, VIDALIS I, STEELE D, et al. Surface hydrophilic modification of RO membranes by plasma polymerization for low organic fouling. Journal of Membrane Science, 2011, 369(1/2): 420¨C428.
[4] YANG C M, CHOI W H, NA B K, et al. Capacitive deionization of NaCl solution with carbon aerogel-silicagel composite electrodes. Desalination, 2005, 174(2): 125¨C133.
[5] WELGEMOED T J, SCHUTTE C F. Capacitive deionization dechnology™: an alternative desalination solution. Desalination, 2005, 183(1/2/3): 327¨C340.
[6] MURPHY G W, CAUDLE D D. Mathematical theory of electrochemical demineralization in flowing systems. Electrochimical Acta, 1967, 12: 1655¨C1664.
[7] JOHNSON A M , NEWMAN J. Desalting by means of porous carbon electrodes. Journal of the Electrochemical Society, 1971, 118(3): 510¨C517.
[8] FARMER J C, FIX D V, MACK G V, et al. Capacitive deionization of NH4ClO4 solutions with carbon aerogel electrodes. Journal of Applied Electrochemistry, 1996, 26(10): 1007¨C1018.
[9] FARMER J C, FIX D V, MACK G V, et al. Capacitive deionization of NaCl and NaNO3 solutions with carbon aerogel electrodes. Journal of the Electrochemical Society, 1996, 143(1): 159¨C169.
[10] XU P, DREWES J E, HEIL D, et al. Treatment of brackish produced water using carbon aerogel-based capacitive deionization technology. Water Research, 2008, 42(10/11): 2605¨C2617.
[11] VILLAR I, ROLDAN S, RUIZ V, et al. Capacitive deionization of NaCl solutions with modified activated carbon electrodes. Energy & Fuels, 2010, 24(6): 3329¨C3333.
[12] ZOU L, MORRIS G, QI D. Using activated carbon electrode in electrosorptive deionisation of brackish water. Desalination, 2008, 225(1/2/3): 329¨C340.
[13] RASINES G, LAVELA P, MAC AS C, et al. Electrochemical response of carbon aerogel electrodes in saline water. Journal of Electroanalytical Chemistry, 2012, 671: 92¨C98.
[14] PENG Z, ZHANG D S, SHI L Y, et al. Comparative electroadsorption study of mesoporous carbon electrodes with various pore structures. The Journal of Physical Chemistry C, 2011, 115(34): 17068¨C17076.
[15] TSOURIS C, MAYES R, KIGGANS J, et al. Mesoporous carbon for capacitive deionization of saline water. Environment Science & Technology, 2011, 45(23): 10243¨C10249.
[16] WANG L, WANG M, HUANG Z H, et al. Capacitive deionization of NaCl solutions using carbon nanotube sponge electrodes. Journal of Materials Chemistry, 2011, 21(45): 18295¨C18299.
[17] LI H B, PAN L K, LU T, et al. A comparative study on electrosorptive behavior of carbon nanotubes and graphene for capacitive deionization. Journal of Electroanalytical Chemistry, 2011, 653(1/2): 40¨C44.
[18] ZHANG D S, SHI L Y, FANG J H, et al. Influence of diameter of carbon nanotubes mounted in flow-through capacitors on removal of NaCl from salt water. Journal of Materials Science, 2006, 42(7): 2471¨C2475.
[19] JIA B P, ZOU L. Graphene nanosheets reduced by a multi-step process as high-performance electrode material for capacitive deionisation. Carbon, 2012, 50(6): 2315¨C2321.
[20] WANG Z, YUE L, LIU Z T, et al. Functional graphene nanocomposite as an electrode for the capacitive removal of FeCl3 from water. Journal of Materials Chemistry, 2012, 22(28): 14101¨C14107.
[21] LI H B, LU T, PAN L K, et al. Electrosorption behavior of graphene in NaCl solutions. Journal of Materials Chemistry, 2009, 19(37): 6773¨C6779.
[22] SINGH V, JOUNG D, ZHAI L, et al. Graphene based materials: Past, present and future. Progress in Materials Science, 2011, 56(8): 1178¨C1271.
[23] STOLLER M D, PARK S, ZHU Y W, et al. Graphene-based ultracapacitors. Nano Letters, 2008, 8(10): 3498¨C3502.
[24] HUMMERS W, OFFEMA R. Preparation of graphitic oxide. Journal of the American Chemical Society, 1958, 80: 1339.
[25] XU Y X, BAI H, LU G W, et al. Flexible graphene films via the filtration of water-soluble. Journal of the American Chemical Society, 2008, 130: 5856¨C5857.
[26] LI H B, ZOU L, PAN L K, et al. Novel graphene-like electrodes for capacitive deionization. Environment Science & Technology, 2010, 44: 8692¨C8697.
[27] WANG H, ZHANG D S, YAN T T, et al. Graphene prepared via a novel pyridine¨Cthermal strategy for capacitive deionization. Journal of Materials Chemistry, 2012, 22(45): 23745¨C23748.
[28] JIA B P, ZOU L. Functionalized graphene as electrode material for capacitive deionization. Science of Advanced Materials, 2013, 5(8): 1111¨C1116.
[29] JIA B P, ZOU L. Wettability and its influence on graphene nansoheets as electrode material for capacitive deionization. Chemical Physics Letters, 2012, 548: 23¨C28.
[30] SI Y, SAMULSKI E T. Synthesis of water soluble graphene. Nano Letters, 2008, 8(6): 1679¨C1682.
[31] DREYER D R , PARK S , BIELAWSKI C W, et al. The chemistry of graphene oxide. Chemical Society Reviews, 2010, 39: 228¨C240.
[32] LIU Y, NIE C Y, LIU X J, et al. Review on carbon-based composite materials for capacitive deionization. RSC Advances, 2015, 5: 15205¨C15225.
[33] WORSLEY M A, KUCHEYEV S O, SATCHER J H, et al. Mechanically robust and electrically conductive carbon nanotube foams. Applied Physics Letters, 2009, 94: 073115.
[34] LI C, SHI G. Three-dimensional graphene architectures. Nanoscale, 2012, 4(18): 5549¨C5563.
[35] WANG Z, DOU B J, ZHENG L, et al. Effective desalination by capacitive deionization with functional graphene nanocomposite as novel electrode material. Desalination, 2012, 299: 96¨C102.
[36] WORSLEY M A, PAUZAUSKIE P J, OLSON T Y, et al. Synthesis of graphene aerogel with high electrical conductivity. Journal of the American Chemical Society, 2010, 132: 14067¨C14069.
[37] WANG H, ZHANG D S, YAN T T, et al. Three-dimensional macroporous graphene architectures as high performance electrodes for capacitive deionization. Journal of Materials Chemistry A, 2013, 1(38): 11778¨C11789.
[38] WEN X R, ZHANG D S, YAN T T, et al. Three-dimensional graphene- based hierarchically porous carbon composites prepared by a dual-template strategy for capacitive deionization. Journal of Materials Chemistry A, 2013, 1(39): 12334¨C12344.
[39] WANG H, SHI L Y, YAN T T, et al. Design of graphene-coated hollow mesoporous carbon spheres as high performance electrodes for capacitive deionization. Journal of Materials Chemistry A, 2014, 2(13): 4739¨C4750.
[40] YANG Z Y, JIN L J, LU G Q, et al. Sponge-templated preparation of high surface area graphene with ultrahigh capacitive deionization performance. Advanced Functional Materials, 2014, 24(25): 3917¨C3925.
[41] XU X T, PAN L K, LIU Y, et al. Facile synthesis of novel graphene sponge for high performance capacitive deionization. Scientific Reports, 2015, 5: 8458.
[42] LILLO-RODENAS M A, CAZORLA-AMOROS D, LINARES- SOLANO A. Understanding chemical reactions between carbons and NaOH and KOH: an insight into the chemical activation mechanism. Carbon, 2003, 41: 267¨C275.
[43] RAYMUNDO-PINERO E, AZAıS P, CACCIAGUERRA T, et al. KOH and NaOH activation mechanisms of multiwalled carbon nanotubes with different structural organisation. Carbon, 2005, 43: 786¨C795.
[44] BARRANCO V, LILLO-RODENAS M A, LINARES-SOLANO A, et al. Amorphous carbon nanofibers and their activated carbon nanofibers as supercapacitor electrodes. Journal of Physical Chemistry C, 2010, 114: 10302¨C10307.
[45] ZHU Y W, MURALI S, STOLLER M D, et al. Carbon-based supercapacitors produced by activation of graphene. Science, 2011, 332: 1537¨C1541.
[46] LI Z, SONG B, WU Z K, et al. 3D porous graphene with ultrahigh surface area for microscale capacitive deionization. Nano Energy, 2015, 11: 711¨C718.
[47] LEE J B, PARK K K, YOON S W, et al. Desalination performance of a carbon-based composite electrode. Desalination, 2009, 237(1): 155¨C161.
[48] LI H B, PAN L K, NIE C Y, et al. Reduced graphene oxide and activated carbon composites for capacitive deionization. Journal of Materials Chemistry, 2012, 22(31): 15556¨C15561.
[49] ZHANG D S, WEN X R, SHI L Y, et al. Enhanced capacitive deionization of graphene/mesoporous carbon composites. Nanoscale, 2012, 4(17): 5440¨C5446.
[50] GAO Y, PAN L K, ZHANG Y P, et al. Electrosorption of FeCl3 solution with carbon nanotubes and nanofibres film electrodes grown on graphite substrates. Surface Review Letters, 2007, 14(6): 1033¨C1037.
[51] LI H B, PAN L K, ZHANG Y P, et al. Ferric ion adsorption and electrodesorption by carbon nanotubes and nanofibres films. Water Science and Technology, 2009, 59(8): 1657¨C1663.
[52] PAN L K, WANG X Z, GAO Y, et al. Electrosorption of anions with carbon nanotube and nanofibre composite film electrodes. Desalination, 2009, 244(1/2/3): 139¨C143.
[53] ZHANG D S, YAN T T, SHI L Y, et al. Enhanced capacitive deionization performance of graphene/carbon nanotube composites. Journal of Materials Chemistry, 2012, 22(29): 14696¨C14704.
[54] LI H B, LIANG S, LI J, et al. The capacitive deionization behaviour of a carbon nanotube and reduced graphene oxide composite. Journal of Materials Chemistry A, 2013, 1(21): 6335¨C6341.
[55] WIMALASIRI Y, ZOU L. Carbon nanotube/graphene composite for enhanced capacitive deionization performance. Carbon, 2013, 59: 464¨C471.
[56] WIMALASIRI Y, ZOU L. Response to "Comments on 'carbon nanotube/graphene composite for enhanced capacitive deionization performance' by Y. Wimalasiri and L. Zou". Carbon, 2015, 81: 847¨C849.
[57] SUN X, XIE M, WANG G K, et al. Atomic layer deposition of TiO2 on graphene for supercapacitors. Journal of The Electrochemical Society, 2012, 159(4): A364.
[58] QIAN Y, LU S B, GAO F L. Preparation of MnO2/graphene composite as electrode material for supercapacitors. Journal of Materials Science, 2011, 46(10): 3517¨C3522.
[59] SEEMA H, KEMP K C, CHANDRA V, et al. Graphene-SnO2 composites for highly efficient photocatalytic degradation of methylene blue under sunlight. Nanotechnology, 2012, 23: 355705.
[60] EL-DEEN A G, BARAKAT N A M, KHALIL K A, et al. Graphene/SnO2 nanocomposite as an effective electrode material for saline water desalination using capacitive deionization. Ceramics International, 2014, 40(9): 14627¨C14634.
[61] EL-DEEN A G, BARAKAT N A M, KIM H Y. Graphene wrapped MnO2-nanostructures as effective and stable electrode materials for capacitive deionization desalination technology. Desalination, 2014, 344: 289¨C298.
[62] PASRICHA R, GUPTA S, SRIVASTAVA A K. A facile and novel synthesis of Ag-graphene-based nanocomposites. Small, 2009, 5(20): 2253¨C2259.
[63] ZHENG L, ZHANG G N, ZHANG M, et al. Preparation and capacitance performance of Ag-graphene based nanocomposite. Journal of Power Sources, 2012, 201: 376¨C381.
[64] CAI P F, SU C J, CHANG W T, et al. Capacitive deionization of seawater effected by nano Ag and Ag@C on graphene. Marine Pollution Bulletin, 2014, 85(2): 733¨C737.
[65] ZHU C Z, GUO S J, WANG P, et al. One-pot, water-phase approach to high-quality graphene/TiO2 composite nanosheets. Chemical Communications, 2010, 46(38): 7148¨C7150.
[66] YIN H J, ZHAO S L, WAN J W, et al. Three-dimensional graphene/ metal oxide nanoparticle hybrids for high-performance capacitive deionization of saline water. Advanced Materials, 2013, 25(43): 6270¨C6276.
[67] EL-DEEN A G, CHOI J H, KIM C S, et al. TiO2 nanorod-intercalated reduced graphene oxide as high performance electrode material for membrane capacitive deionization. Desalination, 2015, 361: 53¨C64.
[68] LAI L F, YANG H P, WANG L, et al. Preparation of supercapacitor electrodes through selection of graphene surface functionalities. ACS Nano, 2012, 6(7): 5941¨C5951.
[69] ZHOU Y, QIN Z Y, LI L, et al. Polyaniline/multiwalled carbon nanotube composites with core-shell structures as supercapacitors electrode materials. Electrochimica Acta, 2010, 55(12): 3904¨C3908.
[70] LI Q. Application of polyaniline modified graphite electrodes for capacitive deionization of aqueous NaCl solution. Asian Journal of Chemistry, 2010, 22(10): 8126¨C8130.
[71] YAN C J, KANATHTHAGE Y W, SHORT R, et al. Graphene/ polyaniline nanocomposite as electrode material for membrane capacitive deionization. Desalination, 2014, 344: 274¨C279.
[72] WU Q, XU Y X, YAO Z Y, et al. Supercapacitors based on flexible graphene/polyaniline nanofiber composite films. ACS Nano, 2010, 4(4): 1963¨C1970.
[73] WANG M, HUANG Z H, WANG L, et al. Electrospun ultrafine carbon fiber webs for electrochemical capacitive desalination. New Journal of Chemistry, 2010, 34(9): 1843¨C1845.
[74] ZHOU Z P, WU X F, FONG H. Electrospun carbon nanofibers surface-grafted with vapor-grown carbon nanotubes as hierarchical electrodes for supercapacitors. Applied Physics Letters, 2012, 100: 023114¨C023115.
[75] BAI Y, HUANG Z H, YU X L, et al. Graphene oxide-embedded porous carbon nanofiber webs by electrospinning for capacitive deionization. Colloids and Surfaces A: Physicochemial and Engineering Aspects, 2014, 444: 153¨C158.
[76] DONG Q, WANG G, QIAN B, et al. Electrospun composites made of reduced graphene oxide and activated carbon nanofibers for capacitive deionization. Electrochimica Acta, 2014, 137: 388¨C394.