硬脂酸湿法表面改性氢氧化镁阻燃剂的研究* yd17223
姬连敏1, 2, 李丽娟1, 陈大福1, 聂峰1, 曾忠民1, 宋富根1 1. 中国科学院青海盐湖研究所, 青海西宁810008; 2. 中国科学院研究生院
收稿日期: 2008- 04 - 03
* 基金项目: 中国科学院科技支青资助项目( ZQ-2006-01) ; 青海省科技厅资助项目( 2005-G-165)。
作者简介: 姬连敏( 1982- ), 女, 硕士研究生, 主要从事无机材料研究, 已发表论文2篇。
联系人: 李丽娟 联系方式: li lj @ isl. ac. cn
原载:无机盐工业2008/9;13-16
【摘要】 主要研究了硬脂酸(SA)湿法表面改性普通氢氧化镁的工艺过程, 其改性效果由活化指数H 进行表征。研究了不同反应温度、搅拌转速、反应时间对活化指数的影响, 同时, 利用FT- IR, SEM, TG 对硬脂酸表面改性的氢氧化镁进行表征。结果表明: 当反应温度为85~ 90℃、搅拌转速为400 r/min、反应时间3 h、硬脂酸用量为2%(占氢氧化镁干粉的质量分数)时, 其活化指数达到96%; 普通氢氧化镁由亲水性完全转变成亲油性; 改性后的氢氧化镁分散性更好, 热分解温度更高。FT- IR, TG分析表明: 硬脂酸分子在氢氧化镁粉体表面发生吸附键合, 形成了新的化学键。
【关键词】硬脂酸(SA ); 氢氧化镁; 阻燃剂
【中图分类号】TQ132. 2. . 文献标识码: A. . 文章编号: 1006- 4990(2008) 09-0013-04
氢氧化镁表面改性研究是通过表面改性剂改变氢氧化镁表面极性, 降低氢氧化镁填料的表面能, 使之趋于聚合物的表面能数值。表面活性剂有阴离子型、阳离子型和非离子型, 其分子的一端为长链烷基, 与聚烯烃分子链有一定相容性; 另一端为羧基、醚基或金属盐等极性基团, 可与无机填料表面发生化学作用或物理化学吸附, 从而有效地改性填料表面[1]。硬脂酸是一种最常用的表面改性剂, 价格低廉。关于使用硬脂酸改性Al(OH)3, Mg(OH)2的报道[2-6]很多, 其作用机理是依靠硬脂酸的酸性基团. COOH与无机填料表面的碱性基团发生作用,反应生成的硬脂酸盐停留在无机粒子表面, 起到表面改性的作用。硬脂酸及其盐对Mg(OH)2的表面改性提高了粉体的分散行为和界面相容性, 改善了复合材料的力学性能。针对青海省某镁盐公司的技术需求, 以硬脂酸为表面改性剂, 对普通型Mg(OH)2进行湿法表面改性。
1. 实验
1. 1. 原料及仪器
普通氢氧化镁(D50 = 6. 435µm ) , 由青海昆仑镁盐有限责任公司提供; 硬脂酸(SA) , 分析纯, 莱阳市双双化工有限公司生产。
美国热电公司NEXUS 型傅里叶红外光谱仪,KBr压片; 日本JEOL 公司的JSM- 5610LV 型低真空激光扫描电子显微镜; 法国SETARAM 公司TGDTA92型热分析仪, 加热速率10℃/min, 高纯氮气(99. 99% )保护, 容器为刚玉坩埚。
1. 2. 实验原理
1. 2. 1. 硬脂酸表面包覆反应
准确称取一定量氢氧化镁原料, 配成质量分数为10%的料浆, 搅拌混合均匀。加热至反应温度,加入一定量硬脂酸, 反应至规定时间, 自然冷却至室温。真空抽滤, 滤饼用蒸馏水洗涤3次, 每次用水量15mL。放入110℃烘箱中干燥, 冷却至室温, 称重,研磨至粒度< 150µm为成品。
1. 2. 2. 活化指数的测定
称取10g改性氢氧化镁, 过孔径75µm 筛, 从中准确称取5 g,取600mL烧杯, 加入300mL蒸馏水, 将样品倒入其中, 搅拌均匀, 静置24 h。将沉降于烧杯底部的样品过滤、抽干, 在110℃下干燥10 h。在干燥器中冷却至室温, 称重。用原样品的质量减去沉降于烧杯底部的样品质量, 即可得到漂浮部分的质量, 由公式(1)即可计算出活化指数H。
H = (样品中漂浮部分的质量/样品总质量) × 100% (1)
未经处理的氢氧化镁H = 0, 活化处理完全的氢氧化镁H = 100%。由0~100%的变化可反应出活化程度由小至大的过程, 从而得知活化效果的情况。
2. 结果与讨论
2. 1. 改性条件对活化指数的影响
2. 1. 1. 反应温度对活化指数的影响
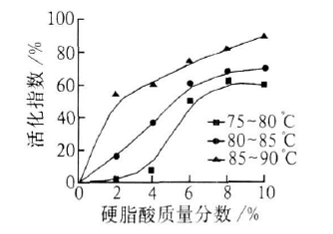
硬脂酸的熔点为70~71℃ , 当低于此温度时,大多数硬脂酸不能熔化, 固体硬脂酸不能起到很好的改性作用。当温度高于71℃时, 硬脂酸为液体,才能达到较好的改性效果。试验表明: 当温度大于90℃时, 料浆沸腾, 为本试验的温度上限。将温度分为3段: 75~80℃, 80~85℃, 85~90℃, 氢氧化镁料浆质量分数为10%, 搅拌转速为400 r /min, 反应时间为45min, 活化指数随硬脂酸质量分数的变化曲线如图1。
|
|
|
图1. 反应温度和硬脂酸质量分数对活化指数的影响 |
由图1 可明确看出: 相同反应温度下, 活化指数随硬脂酸质量分数的增加而增加。同一硬脂酸质量分数下, 随着反应温度的升高, 其活化指数呈上升趋势。75~80℃时的活化指数最低, 改性效果最差; 85~90℃时的活化指数最高, 硬脂酸改性氢氧化镁的活化效果最佳。主要是由于温度相对较低时, 反应物系的粘度相对较大, 以致降低物料混合以及传质的效果, 同时可能降低M g(OH)2 颗粒的表面吸附效果; 当温度升高时, 物料混合及其传质过程加快, 反应速率同时加快, 表面吸附更完全。由此确定最佳改性温度为85~90℃。
2. 1. 2. 搅拌转速对活化指数的影响
在硬脂酸包覆氢氧化镁的反应过程中, 连续搅拌可以加快物料混合, 促进过程传质, 使硬脂酸更充分地分散在氢氧化镁颗粒表面, 致使包覆更加完全。
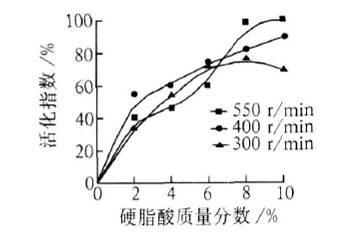
氢氧化镁料浆质量分数为10%, 反应温度为85~90℃, 反应时间为45min, 不同搅拌转速下, 活化指数随硬脂酸质量分数的变化曲线如图2。
|
|
|
图2. 搅拌转速对活化指数的影响 |
由图2看出: 硬脂酸质量分数≤7% 时, 转速为400 r/min的活化指数最高, 而转速为550 r /min的活化指数较低。当硬脂酸质量分数≥8%时, 转速为400 r/min的活化指数降低。原因可能是由于改性剂在部分Mg(OH)2 颗粒表面的吸附由单分子层转变为多层物理吸附, 部分极性基团朝外[7] , 使得活化指数降低; 同时由于颗粒表面含有少量有机溶剂时, 颗粒之间更易发生聚块, 因聚块尺寸比单个颗粒大得多而需经历聚块减小、破裂最终被流动的液体卷入下拉进入搅拌槽内的过程, 因此需更高的搅拌转速才能达到颗粒的临界悬浮[8]。转速为300 r/m in的活化指数总体较低。这是因为硬脂酸为油性的有机质, 不溶于水, 转速较低时, 部分硬脂酸不能较好地被混到料浆中; 较低的搅拌转速, 硬脂酸改性剂与氢氧化镁颗粒表面接触不完全。当增大搅拌转速时, 可以提高能量消耗速率, 加快物料混合过程, 增大传质和传热系数, 促使吸附、键合过程的完成。但是当搅拌转速增大到一定的程度, 二次过程的影响可能开始显现出来, 同时转速过快还会使剪切力变大, 一方面破坏颗粒间的表面吸附, 另一方面也会引起氢键等化学结合力的断裂造成二次团聚, 导致氢氧化镁活化效果降低[9]。因此, 要达到良好的分散效果, 必须选择适当的搅拌转速, 最佳搅拌转速为400 r/min。
2. 1. 3. 不同反应时间对活化指数的影响
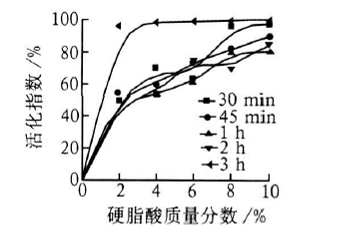
氢氧化镁料浆质量分数为10%, 反应温度为85~90℃ , 反应转速为400 r/min, 不同反应时间下, 活化指数随硬脂酸质量分数的变化曲线如图3。
|
|
|
图3. 反应时间对活化指数的影响 |
从图3看出, 反应时间为30、45min与1, 2 h的活化指数相差不多, 改性效果相当; 当反应时间达3h时, 活化指数突然增大。硬脂酸质量分数为2% 时,活化指数就已达到96%, 再增加硬脂酸质量分数,活化指数基本不变, 氢氧化镁被硬脂酸包覆几乎完全, 氢氧化镁由亲水性转变成亲油性。这表明改性剂硬脂酸与氢氧化镁颗粒在经过一个较长的反应时间(3h)后, 硬脂酸在氢氧化镁粉体表面附着均匀,改善了氢氧化镁颗粒的分散性; 与此同时, 硬脂酸与氢氧化镁还可能发生“弱酯化反应”[4], 形成较稳定的化学键。
2. 2. 硬脂酸改性Mg(OH)2的性能
2. 2. 1. 红外光谱分析结果
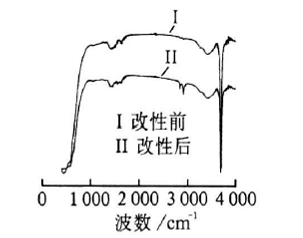
Mg(OH)2粉体改性前后的红外谱图如图4,
|
|
|
图4. M g( OH ) 2粉体改性前后的红外谱图 |
曲线Ⅰ是改性前Mg(OH)2的红外谱图, 曲线Ⅱ是最佳改性工艺条件下的Mg(OH)2的红外谱图。由图4可以看出, 3 699 cm-1处为缔合-OH 的特征吸收峰; 1 630 cm-1 处为结晶水的吸收峰, 这表明Mg(OH)2 粉体中含有少量的水分; 改性后的Mg(OH)2在2 924. 9, 2 850. 1 cm-1处出现了甲基的不对称伸缩振动和亚甲基对称伸缩振动的吸收峰,在1 469. 7 cm-1处也出现甲基、亚甲基有机官能团的吸收峰, 值得注意的是, 曲线Ⅱ中1 574 cm-1处出现硬脂酸盐中羧酸根阴离子[CH3(CH2)16 COO- ]的C=O 键不对称伸缩振动[6,10]。这表明硬脂酸分子与氢氧化镁发生吸附键合, 形成了新的化学键,氢氧化镁表面被有机化。
2. 2. 2. 扫描电镜测试结果
为了研究硬脂酸对Mg(OH)2在干燥状态下分散性的影响, 对改性前后的Mg(OH)2粉体进行了SEM 观察, 结果如图5所示。
|
|
|
a. 改性前. . . . . . . b. 改性后 |
|
图5. 改性前后氢氧化镁的SEM 图谱 |
由图5( a)可以看出,未改性的氢氧化镁团聚程度较严重, 这是由于Mg(OH)2的粒径较小, 具有较大的比表面积和较高的比表面能, 容易吸附周围其他颗粒来降低其表面能, 使单个的Mg(OH)2颗粒不能在干燥状态下稳定存在。由图5(b)可看出, 改性后的氢氧化镁粉体表面包覆了一层有机质, 减小了其极性, 降低了粉体颗粒的表面能, 使粒子处于较稳定的分散状态。
2. 2. 3. Mg (OH)2的热稳定性
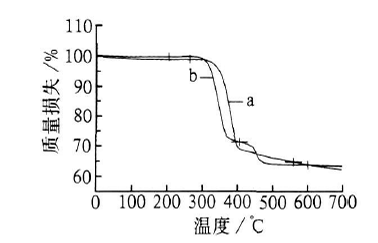
图6为Mg(OH)2改性前后的热分析谱图,
|
|
|
图6. 改性前后Mg(OH)2 的TG谱图 |
图6(a)为改性前Mg(OH)2的TG曲线。从图6可以看出, Mg (OH)2有一个很强的质量损失峰, 主要是Mg(OH)2受热分解。在263. 0~558. 5℃, 质量损失为34. 04% , 稍大于理论质量损失30. 89%, 原因可能有两种: 1) 样品中含有少量的物理、化学吸附水所致; 2)所选择的起始与终止的分解温度范围不同所致, 因为选择的分解温度范围越大, 质量损失值就越大。研究表明: 样品在质量损失突变点340℃之前就已经开始分解, 故将分解温度区间选择为
263. 0~558. 5℃。
图6(b) 为改性后Mg (OH)2的TG 曲线, 从图6(b)可以看出, 存在2 个明显的吸热峰, 203. 4 ~405. 5℃ 时有1个很强的吸热峰, 主要是M g(OH)2受热分解, 质量损失为28. 37% ; 405. 5~600. 4℃有一中等强度的吸热峰, 起始分解温度443℃, 最大分解温度464℃, 质量损失为7. 53%, 这主要是改性后生成的硬脂酸镁的分解, 说明改性剂硬脂酸与Mg(OH)2 表面是化学作用[11] 。硬脂酸在高于160℃时开始分解, 当温度达到600℃时, 质量损失接近100% [12] ; 而由图6 (b) 可以明显看出:
300℃之前没有任何吸热峰, 说明改性后的Mg(OH)2中不存在未参与改性(游离或吸附)的硬脂酸分子。
3. 结论
1)通过试验确定最佳反应条件, 即氢氧化镁料浆质量分数为10% ; 反应温度为85~90℃; 搅拌转速为400 r /min; 反应时间3 h; 硬脂酸用量为2%(占氢氧化镁干粉的质量分数); 其活化指数达到96%。
2)红外光谱结果表明: 1 574 cm-1处出现硬脂酸盐中所含羧酸根阴离子[CH3 (CH2) 16COO- ]的C=O 键吸收峰。这表明硬脂酸分子与氢氧化镁粉体表面发生吸附键合, 形成了新的化学键。
3)扫描电镜研究表明改性后的氢氧化镁, 粒子表面能降低, 其分散性更好。
4)热分析结果表明: 改性剂硬脂酸与Mg(OH)2表面发生化学作用, 生成硬脂酸镁; 同时发现改性后的Mg(OH)2中不存在未参与改性(游离或吸附)的硬脂酸分子。
参考文献
[1]. 杨森, 王少会, 熊伟, 等. 无机填料的表面改性研究进展[J]. 现代塑料加工应用, 2006, 18( 5 ): 53- 56.
[2]. 刘丽君, 郭奋, 陈建峰, 等. 纳米氢氧化铝的表面改性研究[J].北京化工大学学报, 2004, 31(3): 22-26.
[3]. 王子云, 郭奋, 陈建峰, 等. 纳米Al(OH)3表面改性及其在EVA中的阻燃应用[J]. 北京化工大学学报, 2006, 33(4): 9- 12.
[4]. 黄宏海, 田明, 梁文利, 等. 硬脂酸改性M g( OH ) 2的机理及对EVA性能的影响[J]. 北京化工大学学报, 2006, 33 (2) : 50 -54.
[5]. 阎修川, 张桂芹, 马培华, 等. 氢氧化镁粉体的表面改性研究[J]. 无机盐工业, 2006, 38( 8 ): 17- 19.
[6]. 欧乐明, 罗伟, 冯其明, 等. 硬脂酸改性氢氧化镁及表征[J]. 中国非金属矿工业导刊, 2007(2) : 35-38.
[7]. 于才渊, 张玉, 张引. 搅拌流化床干燥器流体力学性能研究[J]. 化学工程, 2006, 34 ( 8) : 28- 30.
[8]. 包雨云, 龙建刚, 高正明, 等. 上浮颗粒特性对三相搅拌槽内固-液悬浮及气-液分散的影响[J]. 高校化学工程学报, 2006,
20 (1) : 25-30.
[9]. 赵建海, 李毓, 高富, 等. 撞击流制备高纯纳米氢氧化镁技术研究[J]. 无机盐工业, 2007, 39 ( 8) : 22 - 24.
[10] . H esselV, D etem p le P, Geiger J F, et a.l Low - tem perature plasma treatment of magnesium stearate Langmuir - B lodgett films[J]. The Solid Film s, 1996, 286(1/2): 241-251.
[11]. 毋伟, 陈建锋, 卢寿慈. 超细粉体表面修饰[M]. 北京: 化学工业出版社, 2004: 197.
[12]. Jaw Kuen-Shan, H su Chung-King, Lee J inn-Shinng. The thermal decomposition behaviors of stearic acid, paraffin wax and poly-vinyl butyral[J]. Thermochimica Acta, 2001, 367: 165-168.