茉莉香精微胶囊的结构调控与性能研究yd13920
张美艳,王炜,钟毅 东华大学,上海201620
收稿日期:2010-08-10
作者简介:张美艳(1986-),女,山东菏泽人,硕士,研究方向为芳香保健面料的开发与性能研究
原载:印染助剂2011年6月;31-34
【摘要】用乳液聚合法制备了以茉莉香精为囊芯、蜜胺树脂为囊壁的缓释性微胶囊,通过改变工艺因素实现对微胶囊结构进行调控,确定了制备缓释性茉莉香精微胶囊的最佳工艺条件:pH值4.5,乳化剂用量15.4%,乳化时间10 min,乳化剪切速率16 000 r/min,芯壁比为1:1。借助SEM观察自制香味微胶囊的形貌特征,并用FTIR谱图表征了茉莉香精及微胶囊的包囊情况,微胶囊的包覆率达82.4%。
【关键词】 香精;蜜胺树脂;微胶囊;乳液聚合法
【中图分类号】TQ610.4 文献标识码:A 文章编号:1004-0439(2011)06-0031-04
香味产品有健身、防病作用。经现代科学研究证明,香味对人的生理、心理会产生不同程度的奇妙影响,某些特定的香味刺激人的嗅觉器官后,会对人起到兴奋、清醒或镇定、止痛的作用,并且可以治疗或预防某些疾病。但香精具有易挥发、易氧化等缺点,其功能得不到充分发挥。香精的微胶囊化即在香精的油微粒周围包覆上一层高分子材料薄膜,可使香气释放速度减慢,达到延长保香期的目的。本文采用乳液聚合,以蜜胺树脂为壁材对茉莉香精进行包覆,制成缓释性香精微胶囊。通过对微胶囊表面结构和性能调控的研究,揭示香味微胶囊的特征、性能和规律,在此基础上总结了微胶囊表面结构控制和生长方法以及对具有优良缓释效果的微胶囊形状和表面结构的控制。
1 试验
1.1 材料及仪器
材料:茉莉香精(上海雅加香精香料有限公司),三羟甲基三聚氰胺、六羟甲基三聚氰胺(上海化工有限公司),高分子乳化剂(试验室自制),冰醋酸、氨水、无水乙醇(均为分析纯),分散剂NNO(~业品)。
仪器:FA25型试验室高剪切分散乳化机(上海弗鲁克流体机械制造有限公司),DK-S12电热恒温水浴箱(上海森信试验仪器有限公司),D2004W 型电动搅拌器(上海司乐仪器有限公司),LS1332型激光粒度分析仪(美国贝克曼库尔特公司),TM-1000型扫描电子显微镜(日本HITACHI公司),640-IR型傅立叶红外光谱仪(美国Varian公司),U- 3310型紫外分光光度计(日本日立公司)。
1.2 茉莉香精微胶囊的制备
精确称取香精、乳化剂和适量蒸馏水,用高剪切分散乳化机于一定转速均化数分钟,用醋酸调节pH值至3~5,用酸碱指示计准确测量此时混合溶液pH值,将混合液倒入三颈烧瓶。室温下滴加部分醚化的三羟甲基三聚氰胺预聚体,并不断搅拌,升温至65℃,保温1.5 h,进行单层造壁;将系统温度冷却至室温,搅拌下滴加六羟甲基三聚氰胺预聚体,升温至75℃,保温2h,进行双层造壁;冷却至室温,用氨水调pH值到7-8。
1.3 测试
红外光谱:采用KBr压片法进行测试,事先用乙醇对微胶囊表面进行清洗,以去除沾在微胶囊表面的香精,使结果准确。
粒径:用滴管吸取少量制得的香精微胶囊混悬溶液(振荡均匀)于小烧杯中,用适量蒸馏水稀释后,置于超声波清洗器中进行振荡分散成单个粒子,然后用激光粒度仪测量香精微胶囊粒子粒径及分布。
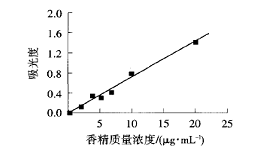
形貌:将微胶囊试样分散于蒸馏水中,涂覆在盖玻片上晾干,真空镀金,用扫描电子显微镜观察其形貌。包覆率:将一定质量浓度的标准茉莉香精-乙醇溶液加入石英比色皿中,在波长190~400 nm进行紫外扫描,间隔1 nm,从扫描图谱中观察吸光度最大的波长,并以此波长下的紫外吸收对应不同质量浓度作标准曲线f图1)。
|
|
|
图1 茉莉香精质量浓度-吸光度标准曲线 |
将反应后的样品用无水乙醇冲洗后,再用清水清洗,真空干燥后,放入装有无水乙醇溶液的圆底烧瓶中,75℃回流1 h后,过滤,将过滤液用乙醇溶液定容到500 mL,测其吸光度。从香精的标准吸收曲线中查出此吸光度所对应的香精质量浓度,从而求出样品中所包覆的香精含量,根据公式计算出包覆率(微胶囊的包覆率是指一定量的囊芯在进行微胶囊化后,被包覆的囊芯量占原始量的比值)。
2 结果与讨论
2.1 FTIR谱图
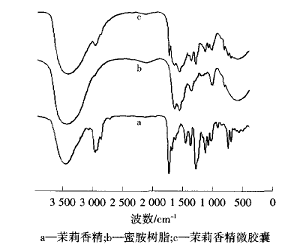
茉莉香精由芳樟醇、乙酸叶醇酯、茉莉酮、对甲酚、吲哚、苯乙醇、α-戊基桂醛二苯乙缩醛等十几种有机小分子组成[1],含-C00R、-0H和C=O等基团,其红外光谱在1 731.24cm-1 处存在强拉伸振动吸收,见图2a.图2b中,3 425.43 cm-1 处为-N-H的伸缩振动吸收峰,3 100 cm-1处为C-H的伸缩振动吸收峰,1 560.05 cm-1 处为-C-0伸缩振动吸收峰,1 363.92cm-1 处为-C-N的伸缩振动吸收峰,1 018.00 cm-1 处为-C-O的伸缩振动吸收峰,813.36 cm-1 处有蜜胺芳杂环的吸收峰,该蜜胺树脂在1 700 cm-1 附近不存在拉伸振动吸收.图2c中,包结后的香精微胶囊经表面去油处理后在1 728.10 cm-1 处出现了拉伸振动吸收,且在814.11 cm-1 处有蜜胺芳杂环的吸收峰,说明蜜胺树脂已包覆了茉莉香精。
|
|
|
图2 茉莉香精、蜜胺树脂及微胶囊的FTIR谱图 |
2.2 影响微胶囊粒径大小、分布及形貌的因素
2.2.1 pH值
蜜胺树脂预聚体在酸性催化剂作用下可发生缩聚反应形成不溶性的分子质量相对较高的蜜胺树脂粒子,在水油界面的表面张力作用下,蜜胺树脂粒子沉积到水油界面形成囊壁,在加热条件下进一步交联固化形成具有一定机械强度的微胶囊[2]试验发现,反应前制备液的pH值对微胶囊粒径、分布及表面结构有很大的影响。
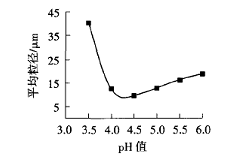
如图3所示,随着pH值的提高,平均粒径变小;当pH值在4.5附近时平均粒径达到最低值,只有8.5 µm左右,但随着pH值的继续增大,微胶囊的平均粒径没有降低,反而增大。因此,选择pH值4.5。
|
|
|
图3 pH值对微胶囊平均粒径的影响 |
2.2.2 乳化剂用量
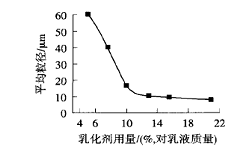
乳化剂是微胶囊制备的关键组分,它对香精液滴起着乳化、分散、稳定等作用,其用量必将影响香精微胶囊的粒径、分布及表面形貌。乳化剂是一种表面活性剂,若用量太少就不能很好地完成乳化,有部分油相芯材没有被包覆在乳化剂里面,这样的乳化液制备成微胶囊后分散液中有大量油滴,影响微胶囊质量和使用[3],用量过多会使制备的微胶囊之间有絮状物相连,并且对香精微胶囊的缓释起到阻碍作用[4]从图4可知,随着乳化剂用量的增加,微胶囊平均粒径逐渐减小;当乳化剂用量15.4%时粒径较小;>15.4%时粒径变化很小,原因是随着乳化剂用量的增加,油水间表面张力逐渐变小,油相容易分散成更小的液滴,但是当乳化剂用量达到一定值后,因表面张力变化很小,粒径变化很小.故乳化剂用量选择15.4%。
|
|
|
图4 乳化剂用量对微胶囊平均粒径的影响 |
2.2. 3 乳化时间
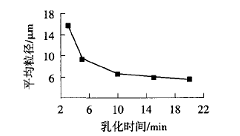
由图5可知,随着乳化时间的延长,平均粒径减小;但乳化10 min后,平均粒径的变化趋于平缓。
|
|
|
图5 乳化时间对微胶囊平均粒径的影响 |
2.2.4 乳化机的剪切速率
在制备茉莉香精微胶囊时,乳化剪切阶段采用高速剪切混合乳化机对茉莉香精、乳化剂、蒸馏水进行高速匀化。乳化剪切作用是打碎、乳化和分散茉莉香精,在一定范围内,当乳化机剪切速率增加时,微胶囊平均粒径减小。原因是随着剪切速率的增加,芯材受到的剪切力增加,使其液滴粒径迅速减小,芯材在体系中分散比较彻底,导致微胶囊平均粒径变小[5]。
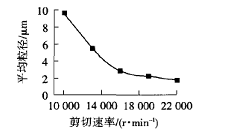
由图6可知,平均粒径随剪切速率的增加而减小。当剪切速率<16 000 r/min时,微胶囊平均粒径曲线下降很快;而随着剪切速率的继续增加,微胶囊平均粒径曲线趋于平缓.说明当剪切速率增加到16 000 r/min时,芯材已经被充分分散成微小液滴,剪切速率的继续增加对粒径的影响就不太明显了.
|
|
|
图6 乳化机的剪切速率对微胶囊平均粒径的影响 |
2.2.5 芯壁比
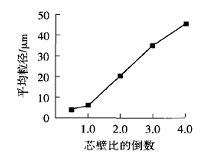
从图7可以看出,芯壁比为2:l和1:1时微胶囊的粒径较小并且相差不大;但是随着微胶囊芯材用量的继续减少,即壁材用量增加,粒径不断增大,且几乎呈线性上升,即香精微胶囊粒径增长几乎与芯壁比成反比。
|
|
|
图7 芯壁比对微胶囊平均粒径的影响 |
由图8可以看出,当芯壁比为2:1时,微胶囊表面浮有大量液滴,香精包覆不完全,原因是芯壁比越小,在电镜下香精微胶囊的外形越大外观越来越不清晰。随着壁材含量的增加,当芯壁比为1:1时香精微胶囊变得饱满、厚实,微胶囊呈规整的球形且表面光滑。当芯壁比为1:3时,制得的微胶囊外形并不呈现圆球形,为不规则形状,且微胶囊表面也不光洁,大量三聚氰胺预聚体自聚产生的杂质沉积在表面.
|
|
|
图8芯壁比对微胶囊形貌的影响 |
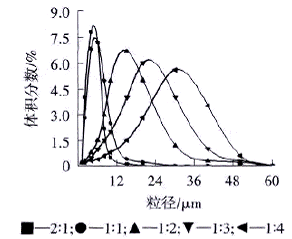
从图9可知,芯壁比>l:l时粒径分布相对较宽,原因是壁材用量相对较多的情况下,芯材分配均匀性相对较差.芯壁比=l:l时,粒径分布较窄,从各方而考虑,选择芯壁比为l:l时较适宜.
|
|
|
图9 芯壁比对微胶囊粒径分布的影响 |
3 结论
(1)蜜胺树脂、茉莉香精和所合成香精微胶囊的FTIR谱图显示蜜胺树脂已将茉莉香精包覆。
(2)微胶囊合成过程中.pH值对微胶囊的成囊性有重要影响,适当提高乳化剂用最、延长乳化时间及提高乳化速度均能使微胶囊的平均粒径有所下降。
(3)制备茉莉香精微胶囊的最佳工艺:pH值4.5,乳化剂15.4%,乳化10 min,剪切速率16000 r/min,芯壁比1:1,制得的微胶囊呈规整的球形且表面光滑,平均粒径较小,粒径分布较集中,微胶囊包覆率达到82.4%。
参考文献:
[I]张福娟,郭丽丽,盛淑玲,茉莉香精乙酸苄酯的催化合成[J]河北化工.2009,32(9);14-15
[2]饯蕾,陈水林,压敏显色微胶囊的合成及性能研究[J]中国纺织大学学报.1996.22(5);1-8
[3]张伦生,吴明华,罗艳,染料微胶囊粒径大小和分布的影响因素[J]印染助剂,2002,19(1);38-40
[4]FELLJT.Delivery
systems for targeting to specific sites in the gastrointestinal tract[J]Journal of Pharmacy and
Pharmacology,1999,3(4);41-48
[5]
DESHPANDE A A,RHODES C T,SHAH H,et al.Controlled-release
drug delivery system for prolonged gastric residence an overview[J]Drug
Development and Industrial Pharmacy,1996,22(6);531-539