ÎÞÈܼÁÓлúºÏ³Éyd13519
ÀîÈêÐÛ Íõ½¨»ù ±±¾©Ê¯ÓÍ»¯¹¤Ñ§Ôº»¯¹¤Ïµ±±¾© 102617
Êո壺2002-08-20 Ð޻أº2002-11-14
×÷Õß½éÉÜ£ºÀîÈêÐÛ ÄÐ 56 Ëê½ÌÊÚ˶ʿ´ÓÊÂÂÌÉ«»¯Ñ§Óë»·¾³±£»¤µÄÑо¿
ÔÔØ£ºhttp://www.hxtb.org »¯Ñ§Í¨±¨ 2003 ÄêµÚ 66 ¾íw020£»1-7
¡¾ÕªÒª¡¿Ðí¶àÓлúºÏ³É·´Ó¦¿ÉÒÔÔÚÎÞÈܼÁÌõ¼þϽøÐÐ ÎÞÈܼÁÓлúºÏ³É¾ßÓз´Ó¦¹ý³Ì¼°ºó´¦Àí
¼òµ¥³É±¾µÍÎÞÎÛȾµÈÓŵ㱾ÎĽéÉÜÁË×ÛÊöÎÞÈܼÁÓлúºÏ³É·´Ó¦µÄ·½·¨ºÍÀàÐÍ
¡¾¹Ø¼ü´Ê¡¿ÎÞÈܼÁ ÓлúºÏ³É ·´Ó¦
1 ÎÞÈܼÁÓлúºÏ³É¸ÅÄî
ÓÉÓÚÈË¿ÚÔö¼ÓÉú²ú·¢Õ¹ÈËÀà»î¶¯¼Ó¾çʹµØÇòÉú̬»·¾³Êܵ½µÄÎÛȾÈÕÒæÑÏÖØÆäÖÐÐí¶àÎÊÌâÓëÈËÀàºÏ³ÉµÄ»¯Ñ§ÎïÖʵÄÉú²úºÍʹÓÃÓйØ20 ÊÀ¼Í90 Äê´úÐËÆðµÄÂÌÉ«»¯Ñ§Á¦Í¼¿Ë·þÔÚÉú²úºÍʹÓû¯Ñ§ÎïÖʵĹý³ÌÖжԻ·¾³Ôì³ÉµÄÎÛȾÔÚÓлú»¯Ñ§ÎïÖʵĺϳɹý³ÌÖÐ(ÓÈÆäÊǹÌÌåÎïÖʲÎÓëµÄ·´Ó¦)ʹÓÃÓлúÈܼÁÊǽÏΪÆÕ±éµÄÕâЩÓлúÈܼÁ»áɢʧµ½»·¾³ÖÐÔì³ÉÎÛȾ¸÷¹ú»¯Ñ§¼Ò´´Ôì²¢Ñо¿ÁËÐí¶àÈ¡´ú´«Í³ÓлúÈܼÁµÄÂÌÉ«»¯Ñ§·½·¨ÈçÒÔˮΪ½éÖÊÒÔ³¬ÁÙ½çÁ÷Ìå(ÈçCO2)ΪÈܼÁ[1] ÒÔÊÒÎÂÀë×ÓÒºÌåΪÈܼÁµÈ·½·¨[2,3] ¶ø×î³¹µ×µÄ·½·¨ÊÇÍêÈ«²»ÓÃÈܼÁµÄÎÞÈܼÁÓлúºÏ³É¡£
Æäʵ´ÓÇ°²¢²»ÊÇûÓÐÎÞÈܼÁÓлúºÏ³É·´Ó¦Ðí¶àÆøÌå»òÒºÌå²Î¼ÓµÄ·´Ó¦±ãÊÇÔÚÎÞÈܼÁϽøÐеĵ«Ã÷È·µØÓÐÒâʶµØÌá³öÎÞÈܼÁÓлúºÏ³É¸ÅÄÊÇ20 ÊÀ¼Í90 Äê´úÎÞÈܼÁÓлúºÏ³ÉÊÇÂÌÉ«»¯Ñ§ÖеÄÒ»¸öиÅÄîÐÂÌá·¨
1.1 ÎÞÈܼÁÓлúºÏ³ÉµÄÓŵã
ÓÉÓÚ·´Ó¦¹ý³ÌÍêÈ«²»ÓÃÈܼÁ³¹µ×¿Ë·þÁË·´Ó¦¹ý³ÌÖÐÈܼÁ¶Ô»·¾³Ôì³ÉµÄÎÛȾ²»ÓÃÈܼÁÓÐÀûÓÚ½µµÍÉú²ú³É±¾ÎÞÈܼÁºÏ³ÉΪ·´Ó¦ÌṩÁËÓ봫ͳÈܼÁ²»Í¬µÄеķÖ×Ó»·¾³ÓпÉÄÜʹ·´Ó¦µÄÑ¡ÔñÐÔת»¯Âʵõ½Ìá¸ß¿Éʹ²úÎïµÄ·ÖÀëÌá´¿¹ý³Ì±äµÃ½ÏÈÝÒ×½øÐÐÈçÓеķ´Ó¦Íê³ÉºóÓÃÉÙÁ¿Ë®»òÓлúÈܼÁÏ´¾»¼´¿ÉÓеķ´Ó¦µ±¼ÓÈë¼ÆÁ¿±ÈµÄ·´Ó¦ÎïÇÒת»¯ÂÊ´ïµ½100%ʱµÃµ½µÄÊǵ¥Ò»µÄ´¿¾»²úÎï²»±Ø½øÐзÖÀëÌá´¿Òò´ËÎÞÈܼÁÓлúºÏ³ÉÓ¦µ±³ÉΪѡÔñ·´Ó¦½éÖÊʱÊ×ÏȼÓÒÔ¿¼Âǵķ½·¨ÖµµÃ´óÁ¦¼ÓÒÔÑо¿ºÍÌᳫ
1.2 ÎÞÈܼÁÓлúºÏ³ÉµÄÎÊÌâ
ÎÞÈܼÁÓлúºÏ³ÉÒ²ÓÐÆä¹ÌÓеÄȱµãÌرðÊǶԴÓǰʹÓÃÓлúÈܼÁ½ÏΪÆÕ±éµÄ¹ÌÌåÎïÖʲÎÓëµÄ·´Ó¦,»áÓÐÈçÏÂһЩÎÊÌâ(1)·´Ó¦ÄÜ·ñ½øÐÐÒòΪ²Î¼Ó·´Ó¦µÄ·Ö×ÓÖ®¼äÒª½Ó½üµ½Ò»¸öС¾àÀë(Èç<1nm)²Å¿ÉÄÜ·¢Éú·´Ó¦¶ø²»Í¬¹ÌÌå·´Ó¦Îï·ÛÄ©»ìºÏʱ,´ïµ½´Ë¾àÀëµÄÒìÖÖ·Ö×Ó¶ÔËùÕ¼±ÈÀýºÜС,Òò¶øÐí¶à·´Ó¦ÎÞÈܼÁ²»ÄܽøÐÐÐèÒªÒªÑо¿²ÉÓÃʲô·½·¨´Ù½ø·´Ó¦µÄ½øÐÐ(2)É¢ÈÈÎÊÌâÓÐЩ·´Ó¦½øÐÐʱ·ÅÈȶàÔÚÎÞÈܼÁÌõ¼þϾʹæÔÚÉ¢ÈÈÄѵÄÎÊÌâ(3)·ÖÀëÎÊÌâ·´Ó¦Íê³ÉºóÈôµÃµ½µÄÊǹÌÌå»ìºÏÎï½øÐзÖÀëʱÓпÉÄÜÓÖҪʹÓÃÓлúÈܼÁ(4)Òò·´Ó¦ÏµÍ³ÎÞÁ÷¶¯ÐÔ×éÖ¯´ó¹æÄ£µÄ×Ô¶¯»¯Ë®Æ½¸ßµÄÉú²ú½ÏÄÑ
¸÷¹úѧÕß½øÐÐÁË´óÁ¿µÄÎÞÈܼÁÓлúºÏ³ÉÑо¿Ö÷Òª¼¯ÖÐÔÚ¸÷Àà¹ÌÌå·´Ó¦²ÉÓöàÖÖ·½·¨´Ù½ø·´Ó¦Ê¹Ö®ÄÜƽÎȽøÐÐ
2 ÎÞÈܼÁÓлúºÏ³ÉµÄ·´Ó¦·½·¨¼°ÊµÀý
Ϊʹ·´Ó¦(ÌرðÊǹÌÌå·´Ó¦)ÔÚÎÞÈܼÁÌõ¼þÏÂÄܹ»½øÐÐÖ÷Òª²ÉÓÃÈçÏÂһЩ·½·¨±ÈÈçÓÐЩ·´Ó¦Ö»Òª¼ÓÈȾ²Öûò¼ÓÈȽÁ°è»ìºÏ¼´¿É½øÐÐÓÖÈçÓÃÑв§ÑÐÄ¥,Æð·ÛËé¼Óѹ»ìºÏ×÷ÓÃÓÃÇòÄ¥»ú»ò¸ßËÙÕñ¶¯·ÛËéµÈÇ¿Á¦»úе·½·¨ÒÔ¼°Óó¬Éù²¨ÕÕÉäʹ·´Ó¦½øÐеȻúе·½·¨»¹ÓÐÓùâÕÕÉäʹ·´Ó¦½øÐÐÓÃÖ÷Ìå-¿ÍÌå·½·¨ÒÔ·´Ó¦µ×ÎïΪ¿ÍÌåÒÔÒ»¶¨±ÈÀýµÄÁíÒ»ÖÖÊʵ±·Ö×ÓΪÖ÷ÌåÐγɰü½Ó»¯ºÏÎïÈ»ºóÔÙÉ跨ʹµ×Îï·¢Éú·´Ó¦Õâʱ·´Ó¦µÄ¶¨Î»Ñ¡ÔñÐÔ»ò¹âѧѡÔñÐԵȶ¼»áÒòÖ÷ÌåµÄ×÷ÓöøÓÐËù¸Ä±ä»ò¸ÄÉÆ,ÉõÖÁ±ä³ÉÖ»ÓÐÒ»ÖÖÑ¡Ôñ
2.1 ÓÃÇòÄ¥·¨·´Ó¦
ÔÚԲͲÐνðÊôÖÆ·´Ó¦Æ÷ÖмÓÈë½ðÊôÇòºÍÒª½øÐз´Ó¦µÄÎïÖÊʹ·´Ó¦Æ÷Ðýת½øÐÐÑÐÄ¥ÒÔʵÏÖ·´Ó¦£¬Îª³ýÈ¥»·¾³ÎÛȾÎïÖеÄÓк¦ÓлúÂÈ»¯ÎïÈçDDT PCB Âȱ½¶þ¶ñÓ¢µÈ°ÑÎÛȾÎïÓëMg»òCa CaO µÈ»ìºÏÓÃÇòÄ¥·¨ÑÐÄ¥6h ¿ÉÍÑÂÈ[4]£¬ÓÖÈçÏ©°·ÀàÎïÖÊ1 ÓëÎïÖÊ2 ÓÃÇòÄ¥·¨·´Ó¦3h ÔÙ¼ÓÈȵ½80¡ãC 5min 150¡ãC 5min ϵͳ¾Ò»ÏµÁз´Ó¦µÃ²úÎï3[5]
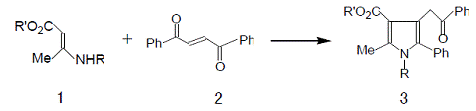
2.2 ÓøßËÙÕñ¶¯·ÛËé·¨·´Ó¦
ÊDZÈÇòÄ¥·¨¸üÇ¿µÄ»úе×÷Ó÷½·¨ÔÚÃÜ·âµÄ²»Ðâ¸ÖÖÆ·´Ó¦Æ÷ÖмÓÈë²»Ðâ¸ÖÇò·´Ó¦Æ÷ÒÔ3500rpm µÄתËÙÐýתʹ¼ÓÈëµÄÎïÖÊ·¢Éú·´Ó¦¡£ÈçC60 µÄ(2+2)¼Ó³ÉÉú³É¶þ¾ÛÌåC120 µÄ·´Ó¦Êǽ«C60 ÓëKCN »òKOAc K2CO3 ¼°Î¢Á¿µÄLi»òNa K µÈ¼î½ðÊôÒ»Æð½øÐиßËÙÕñ¶¯·ÛËéÌõ¼þϵķ´Ó¦ÎÞ»úÎïÊÇ×÷´¥Ã½µÄ·´Ó¦30min ´ïµ½Æ½ºâ¶þ¾ÛÌ庬Á¿Îª30%[6,7]
2.3 ÓÃÀë×ÓÒºÌå´ß»¯·´Ó¦
ÒÔÀë×ÓÒºÌå(BMIM)AlCl4 Ϊ´ß»¯¼Á((BMIM)±íʾ1-¶¡»ù-3-¼×»ùßäßòÑôÀë×Ó) ½øÐд¼»ò·ÓµÄËÄÇâßÁà«»¯·´Ó¦ËÄÇâßÁà«»¯ÊǶಽÓлúºÏ³ÉÖÐ×î³£Óõı£»¤ÓëÈ¥±£»¤·½·¨
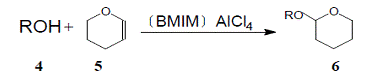
µ±ROH Ϊ»·ÒÑ´¼Ê±ÔÚ25 ·´Ó¦5min ת»¯ÂÊ´ï100%[8] ¸Ã×÷Õß¹²Ñо¿ÁË9 ÖÖ´¼»ò·ÓµÄ·´Ó¦ÆäÖÐ8 ÖÖת»¯ÂÊ´ï100% Àë×ÓÒºÌå¿ÉÓÃÒÒÃÑÝÍÈ¡²¢Ñ»·Ê¹ÓÃ
2.4 Ó¦ÓÃÖ÷Ìå-¿ÍÌå°ü½Ó»¯ºÏÎïµÄ·½·¨
2.4.1 ²»¶Ô³Æ»¹Ô·´Ó¦[9,10]
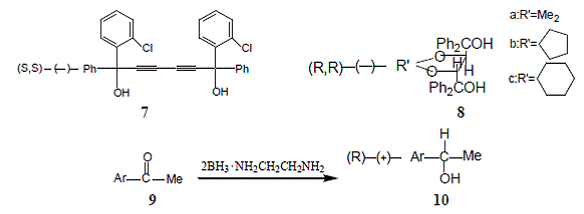
ʹÓÃÓйâѧ»îÐÔµÄÖ÷Ìå½øÐйÌÏ಻¶Ô³Æ»¹Ô·´Ó¦ ¹âѧ»îÐÔµÄ7 »ò8×÷ΪÖ÷ÌåÓëͪ9(¿ÍÌå)µÄ°ü½Ó»¯ºÏÎï½á¾§·ÛÄ©ÓëÅðÍéÒÒ¶þ°·(2BH3 NH2CH2CH2NH2)µÄÅäºÏÎï·ÛÄ©»ìºÏ·´Ó¦¿ÉµÃµ½¹âѧ»îÐԵĴ¼R-(+)-10 ·´Ó¦µÄÊÕÂʼ°¹âѧ»îÐÔ¼û±í1
±í1 ÎÞÈܼÁ²»¶Ô³Æ»¹ÔͪΪ´¼µÄ·´Ó¦ÖвúÎïµÄ²úÂʺ͹âѧ´¿¶È
|
Ö÷Ìå |
9 ÖÐAr |
²úÎï10 |
|
|
²úÂÊ/% |
¹âѧ´¿¶È/ee% |
||
|
(-)7 |
Ph |
96 |
44 |
|
(-)7 |
o-tolyl |
57 |
59 |
|
(-)7 |
1-naphthyl |
20 |
22 |
|
(-)8a |
1-naphthyl |
32 |
22 |
¶Ô»·×´µÄͪ·Ö×Ó11 ÓëÖ÷Ìå8a ÒÔ1:1 µÄ°ü½Ó»¯ºÏÎï·ÛÄ©ÓÃNaBH4 »¹Ô»ìºÏÁ½ÖÖ·ÛÄ©·ÅÖÃ3d ʹ֮·´Ó¦µÃµ½100ee%¹âѧ´¿µÄ(R,R)-(-)-12 ·Ö×ÓÊÕÂÊ54% 55% ·´Ó¦Îï11 ·Ö×Ó×óϽǵÄO Ô×ÓÓëÖ÷Ìå8 ÐγÉÇâ¼ü¹Êδ»¹Ô
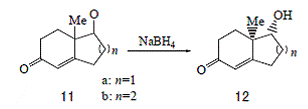
2.4.2 ²»¶Ô³ÆºÏ³ÉÖÐµÄ Wittig ·´Ó¦[11]
ÒÔ·Ö×Ó 8b »ò8c ΪÖ÷ÌåÓëͪÐγɵİü½Ó»¯ºÏÎï½á¾§·ÛÄ©ÓëWittig ÊÔ¼Á14 µÄ·ÛÄ©·´Ó¦²»¶Ô³Æ¹¹ÐÍÑ¡ÔñÐԺܸ߼ûÏÂÁз´Ó¦Ê½
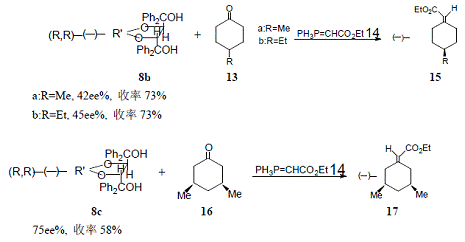
2.5 ¹â»¯·´Ó¦
ÒÔßÁà¤Íª18 Ϊ¿ÍÌ廯ºÏÎï19 ΪÖ÷ÌåÐγɵÄ1:1 °ü½Ó»¯ºÏÎï¾¹âÕÕßÁà¤Íª18 ·¢Éú·Ö×ÓÄÚ»·¼Ó³É·´Ó¦µÃµ½¹âѧ´¿¶ÈΪ100%µÄÄÚõ£°·20[12]
|
|
2.6 ÓÃÑв§ÑÐÄ¥·´Ó¦
2.6.1 ¶þ±½ÒÒ¶þͪ(21)Óë2 ±¶Á¿µÄKOH ÓÃÑ⧻ìºÏÑÐÄ¥ÔÚ80 ·´Ó¦12min ºó»ìºÏÎïÓÃÏ¡ËáÏ´¾»µÃËá22,²úÂÊ90% ±½»·ÉÏÓÐÎüµç×Ó»ùʱ·´Ó¦¼Ó¿ìÓй©µç×Ó»ùʱ·´Ó¦±äÂý[13]
|
|
2.6.2 ȩͪËõºÏ·´Ó¦[14]
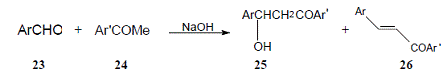
µ±23 ÖÐAr Ϊp-MeC6H4 ºÍ24 ÖÐAr'ΪPh ʱÓëNaOH ÔÚÊÒÎÂÏÂÓÃÑ⧻ìºÏÑÐÄ¥5min ×î³õµÄҺ״Îï±äΪµ»ÆÉ«¹ÌÌå¼ÓË®¹ýÂ˵Ã26(¶Ô¼×»ù²é¶úͪ) ÊÕÂÊ97% ÎÄÏ×[14]¹²Ñо¿ÁË7¸ö¾ßÌåµÄ·´Ó¦¶àÊýÇé¿öÎÞÈܼÁ±ÈÔÚ50%ÒÒ´¼Ë®ÈÜÒºÖз´Ó¦ÊÕÂÊÒª¸ß
2.7 Óó¬Éù²¨ÕÕÉä·´Ó¦
ÎÄÏ×[15]±¨µÀÓÃÃÉÍÑÍÁK-10 µ£ÔصÄFe(NO3)3 ΪÑõ»¯¼Áʹ²®´¼ÖÙ´¼Ñõ»¯ÎªÈ©ºÍͪµÄ·´Ó¦Óó¬Éù²¨ÕÕÉ䷴Ӧʱ¼ä15 60s È©»òͪµÄ²úÂÊ´ï87% 96%
ÎÄÏ×[16]±¨µÀÓÃAl2O3 µ£ÔصĴ×Ëá¼ØKAc Óë1-äåÐÁÍé·´Ó¦Óó¬Éù²¨ÕÕÉ䷴Ӧʱ¼ä2min´×Ëáõ¥µÄ²úÂÊ´ï99%
2.8 ÔÚ¸ÉÔïÆ÷Öз´Ó¦
ÎÄÏ×[17]±¨µÀÓô¼27 Ö®·ÛÄ©ÔÚ¸ÉÔïÆ÷ÖÐÓëHCl ÆøÌå½Ó´¥·´Ó¦5h µÃÏ©28 ²úÂÊ´ï99-100%
|
|
2.9 ¼ÓÈȾ²ÖûòÊÒÎÂϾ²Ö÷´Ó¦[18]
Èç2-¼×»ù»·¼ºÍª(29)Óë¼×»ùÒÒÏ©»ù¼×ͪ(30)ÔÚÎÞÈܼÁÌõ¼þÏ·¢ÉúRobinson Ëõ»··´Ó¦ÈçÏÂ
|
|
ÔÚÊÒÎÂÏ·ÅÖÃ3h ²úÎï31 µÄ²úÂÊΪ25%ÏÔÈ»ÊÒÎÂϾ²ÖÃÄܺÄ×îÉÙ×îΪ¼òÒ×Æä´ÎÊǼÓÈȾ²Öûò¼ÓÈȽÁ°éÏà±ÈÖ®ÏÂÆäËü»úе·½·¨ÄܺĽϸ߻òÒÇÆ÷¶à²Ù×÷½Ï¸´ÔÓ
3 ÎÞÈܼÁÓлúºÏ³É·´Ó¦µÄÀàÐÍ
ÎÄÏ×Öб¨µÀ¹ýµÄÑо¿³É¹¦µÄÎÞÈܼÁÓлúºÏ³É·´Ó¦ºÜ¶à¼¸ºõ°üÀ¨´ó¶àÊýÓлúºÏ³É·´Ó¦µÄÀàÐÍÏÂÃæÁоÙÆäÖÐһЩ½ÏΪµäÐ͵ķ´Ó¦ÀàÐÍ (²»ÔÙһһд³ö¾ßÌåµÄ·´Ó¦ÊµÀý)[19~22]
3.1 ÈÈ·´Ó¦
(1)Ñõ»¯·´Ó¦ÈçBaeyer-Villiger Ñõ»¯·´Ó¦
(2)»¹Ô·´Ó¦ÈçÓÃNaBH4 ʹͪ»¹ÔΪ´¼
(3)Cannizzaro Æ绯·´Ó¦È罫ȩÆ绯Ϊ´¼ºÍËá
(4)¼Ó³É·´Ó¦Èç±Ëغͱ»¯Çâ¼Ó³É,Michael ¼Ó³É
(5)ÏûÈ¥·´Ó¦Èç´¼ÏûÈ¥±äΪϩ
(6)C-C żºÏ·´Ó¦[2+2] [4+2] [6+2]»·¼Ó³É·´Ó¦,°üÀ¨Diels-Alder ¼Ó³ÉȩͪËõºÏ·´Ó¦Dieckmann ËõºÏ·´Ó¦Grignard,Reformasky,Luche ·´Ó¦Wittig ·´Ó¦Ò¶Á¢µÂ·´Ó¦Claisen ·´Ó¦Robinson Ëõ»··´Ó¦Pinacol żºÏ·´Ó¦·ÓÖ®¼äµÄżºÏ·´Ó¦È²»¯ºÏÎïµÄÑõ»¯Å¼ºÏ·´Ó¦C60 µÄ¼Ó³ÉÓëżºÏ·´Ó¦
(7)È¡´ú·´Ó¦°±½âË®½âõ¥½»»»ÃÑ»¯
(8)¾ÛºÏ·´Ó¦
(9)ÖØÅÅÓëÒì¹¹: Pinacol ÖØÅÅÈç¶þ±½ÒÒ¶þͪתλºÍÁÚ¶þÊ崼תλBeckmann ÖØÅÅMeyer Schuster ÖØÅÅChappman ÖØÅÅÒì¹¹»¯
3.2 ¹â»¯·´Ó¦
(1)¶þ¾ÛºÍ¾ÛºÏ
(2)»·»¯
(3)ÖØÅÅÓëÒì¹¹
(4)ÃÑ»¯
(5)È¥ôÊ»ù»¯
(6)²»Í¬·Ö×Ó¼äµÄ¹â»¯¼Ó³É
(7)²»¶Ô³ÆÑ¡ÔñÐԹ⻯·´Ó¦ÊÖÐÔ·Ö×ӵIJ»¶Ô³ÆÑ¡ÔñÐԹ⻯·´Ó¦·ÇÊÖÐÔ·Ö×ÓÔÚÊÖÐÔ°üºÏÎïÖеIJ»¶Ô³ÆÑ¡ÔñÐԹ⻯·´Ó¦·ÇÊÖÐÔ·Ö×ÓÔÚÆäÊÖÐÔ¾§ÌåÖеIJ»¶Ô³ÆÑ¡ÔñÐԹ⻯·´Ó¦µÈµÈ
4 ½áÓï
ÎÞÈܼÁÓлúºÏ³ÉÊÇÂÌÉ«»¯Ñ§ÖеÄÒ»¸öиÅÄî·²Óöµ½ÓлúºÏ³É·´Ó¦,Ê×ÏÈÓ¦¿¼ÂDz»ÓÃÈܼÁÄÜ·ñʵÏÖ·´Ó¦,Ñо¿²»ÓÃÈܼÁÈçºÎʵÏÖ·´Ó¦ÔÚÂÌÉ«»¯Ñ§ÖÐÁíÒ»¸öиÅÄî½Ð»·¾³Òò×ÓÖ¸Éú²úÿµ¥Î»(kg »òmol)µÄ»¯Ñ§²úƷʱÏò»·¾³ÅŷŵķÏÎïÁ¿»·¾³Òò×ÓÓ¦¾¡Á¿¼õСÕâÓ뾡¿ÉÄÜʹÓÃÎÞÈܼÁÓлúºÏ³ÉÆäÔÀíÊÇÏàͬµÄ¶¼ÔÚÓÚ¼õÇáÈËÀàÉú²ú»î¶¯¶Ô»·¾³µÄÎÛȾÓëÆÆ»µµ±È»ÎÞÈܼÁÓлúºÏ³É²»½öÔÚ¼õÇá¶Ô»·¾³µÄÎÛȾÓëÆÆ»µ·½ÃæÓкô¦¶øÇÒʹÓõõ±Ê±ÔÚ½µµÍÉú²ú³É±¾¸Ä½ø»¯Ñ§·´Ó¦µÄÑ¡ÔñÐÔÓëת»¯Âʼò»¯²úÎïµÄ·ÖÀëÌἃµÈ·½ÃæÒ²»áÓкô¦
ÎÞÈܼÁÓлúºÏ³ÉÊÇÒ»Ïî´óÓÐǰ;·Ç³£ÓÐÓõļ¼ÊõÒ»·½ÃæÒÑÑо¿¹ýµÄ³É¹¦ÊµÏÖÎÞÈܼÁÓлúºÏ³É·´Ó¦µÄÀàÐͺͷ´Ó¦ÒѾºÜ¶àÁíÒ»·½ÃæÒÑ·¢Õ¹Á˲»Éٴٽø·´Ó¦µÄ·½·¨(ÓеĿÉÄÜÔö¼ÓÄܺÄ,ÊDz»ÀûµÄ) ʹÈËÃÇÓÐÐÅÐĽøÒ»²½¿ªÕ¹ÎÞÈܼÁÓлúºÏ³ÉµÄÑо¿ÄËÖÁÍƹ㵽Éú²úÖÐÈ¥¿ÉÒÔ˵ʹÓÃÓлúÈܼÁµÄÓлúºÏ³ÉÊÇ19 20 ÊÀ¼ÍµÄ´«Í³·½·¨¶øÎÞÈܼÁÓлúºÏ³ÉÊÇÏÖ´úµÄ¸ü°²È«¸ü»·±£µÄÂÌÉ«»¯Ñ§·½·¨
Ä¿Ç°ÎÞÈܼÁÓлúºÏ³ÉÑо¿Ö÷Òª¼¯ÖÐÔÚʵÑéÊÒʵÏÖ·´Ó¦µÄ»ù´¡Ñо¿É϶ԲúÎïµÄ·ÖÀëÌá´¿Ñо¿²»¶à¶ÔʵÏÖÎÞÈܼÁÓлúºÏ³É·´Ó¦µÄ¹æÂÉÈÏʶ²»×ã¶Ô½øÒ»²½Íƽøµ½Éú²úÖеÄÓ¦ÓÃÑо¿¸üÉÙÕâÒ²ÊÇÕý³£µÄÏÖÏó,ÒòΪÎÞÈܼÁÓлúºÏ³ÉÕâÒ»¸ÅÄîÐγÉʱ¼ä²»³¤¿ÉÒÔÔ¤ÆÚ½ñºó¶ÔÕâЩ·½ÃæµÄÑо¿»áµÃµ½¼ÓÇ¿
²Î¿¼ÎÄÏ×
[1] ¿×·²Ö¾, Ìィ»ª, ½ð×ÓÁÖ. ʯÓÍ»¯¹¤, 2002,31(5):387~392.
[2] ÀîÈêÐÛ, Íõ½¨»ù. »¯¹¤½øÕ¹, 2002, 21(1):43~48.
[3] R Li, J Wang. Chemical Journal on Internet 2002,4(4):044017rc.
[4] S A Rowlands, A K Hall, P G McCormick et al. Nature, 1994, 367:223.
[5] G Kaupp, J Schmeyers, A Kuse et al. Angew. Chem. Int. Ed. Engl., 1999, 38:2896~2900.
[6] G W Wang, K Komatsu, Y Murata et al. Nature, 1997, 387:583~586.
[7] K Komatsu, G W Wang, Y Murata et al. J. Org. Chem., 1998, 63:9358~9366.
[8] V N Vasudevan, S V Rajender. Chem. Commun., 2002:342~343.
[9] F Toda, K Mori. Chem. Commun., 1989:1245~1246.
[10] F Toda, K Tanaka. Tetrahed. Lett., 1988, 29:1245~1248.
[11] F Toda, H Akai. J. Org. Chem., 1990, 55:3446~3450.
[12] F Toda, K Tanaka.Tetrahed. Lett., 1988, 29:4299~4302.
[13] F Toda, K Tanaka, Y Kagawa et al. Chem. Lett., 1990:373~377.
[14] F Toda, K Tanaka, K Hamai. J. Chem. Soc., Perkin Trans., 1990:3207~3209.
[15] R S Varma, R Dahiya. Tetrahed. Lett., 1997, 38:2043~2046.
[16] G Barm, A Loupy, M Majdoub et al. Tetrahedron, 1990, 46:5167~5170.
[17] F Toda, H Takumi, M Akehi. Chem. Commun., 1990:1270~1271.
[18] H Miyamoto, S Kanetaka, K Tanaka et al. Chem. Lett., 2000:888~891.
[19] K Tanaka, F Toda. Chem. Rev., 2000, 100:1025~1074.
[20] K Tanaka, N Takamoto, Y Tezuka et al. Tetrahedron, 2001, 57(17):3761~3767.
[21] »§ÌïܽÈý·ò. , 2001, 46(7):41~48.
[22] СËɽTÒ». »¯Ñ§×Ü˵(ÈÕ), 2000,(47):163~175._