茉莉香精微胶囊的制备和表征yd11808
潘勇军1 薛寒兵1
张飞1 郑成赋2 1.武汉科技学院纺织与材料学院武汉430073 2.华中科技大学国家防伪工程技术项目中心 武汉430074
收稿日期:2009-06-07
作者简介:潘勇军,男,讲师,研究方向:多相聚合物
原载:染整技术2009/11;33-37
【摘要】通过界面聚合方法,在水包油体系中以聚氨酯为囊壁材料将香精包覆形成一种微胶囊,考察了乳化剂用量、搅拌速度对微胶囊的形成、粒径大小和分布及对微胶囊包埋率和缓释性能的影响,确定了制备缓释型香精微胶囊的最佳工艺条件,用红外光谱表征了香精及其微胶囊的包裹情况,并用紫外分光光度计测定了其缓释性能,将制得的香料微胶囊在毛巾和棉布上进行芳香整理。
【关键词】缓释;聚氧酯;微胶囊:界面聚合;芳香整理
【中图分类号】TSl95.2 文献标识码:B 文章编号:1005―9350(2009)l1-0033-05
l 前言
微胶囊化技术(Microencapsulation)是指将某一目的物(芯或内相)用各种天然的或合成的高分子化合物连续薄膜(壁或外相)完全包覆起来,而对目的物的原有化学性质丝毫无损,然后逐渐地通过某些外部刺激或缓释作用使目的物的功能再次在外部呈现出来,或者依靠囊壁的屏蔽作用起到保护芯材的作用。微胶囊技术是一项应用十分广阔的工艺技术,它可以改善被包裹物质的物理性质(颜色、外观、表观密度、溶解性),提高物质的稳定性,使物质免受环境的影响,改善被包裹物质的反应活性、耐久性(延长挥发性物质的贮存时间、压敏性、热敏性和光敏性,减少有毒物质对环境造成的不利影响,根据需要持续释放物质进入外界环境等,上述功能使得微胶囊化成为许多工业领域中的一种有效的商品化方法。微胶囊化可以使许多传统的工艺过程得到简化,同时它也使许多用通常技术手段无法解决受热、光、氧化的影响,避免有效成分挥发,有效控制香味物质的释放,从而扩大了的工艺问题得到解决[1]。缓释型香精微胶囊还可应用于纺织染整工业的加香整理以及日化产品、医药以及香味广告等领域[2-6]。本文通过界面聚合方法,在水包油体系中以聚氨酯为囊壁材料将茉莉香精包覆形成一种微胶囊,研究其最佳工艺条件,进行微胶囊基本性能的测试及在纺织品上进行芳香性整理。
2 实验部分
2.1 原材料
2,4-甲苯二异氰酸酯(TDI),分析纯,武汉市江北化学试剂厂生产:聚乙二醇(PEG-1000),化学纯,中国医药集团上海化学试剂公司生产;吐温-80(Tween-80),化学纯,天津市科密欧化学试剂开发中心生产;白猫牌日用茉莉香精,化学纯,浙江黄岩香料厂生产;低温粘合剂,化学纯,上海化学试剂公司生产;柔软剂JFC,化学纯,天津市科密欧化学试剂开发中心生产。
2.2 实验步骤
本试验选用了2,4-甲苯二异氰酸酯(TDI)和聚乙二醇(PEG)作为原料,制备分两步进行,第一步是预聚物的制备,将PEG溶解在丙酮中,完全溶解后在室温的情况下加入TDI,一定时间(0.5~l h)后停止反应。第二步是微胶囊的制备,将一定比例的香料和第一步所得预聚物混合均匀[香料/预聚物溶液=1:10(体积比)],在室温和快速搅拌的情况下加入到含有乳化剂的水溶液中[乳化剂/水=1:lO(体积比)],形成水包油的乳浊液体系,乳化到微胶囊粒径合乎要求后加入扩链剂(邻苯二酚/TDI的摩尔比=1:4),恒温60℃条件下搅拌继续一定时间(1.5~2 h),放慢搅拌速度,冷却至室温,静置,过滤。
2.3 分析测试
(1)微胶囊红外光谱的测定
用苯溶解干燥好的微胶囊,其溶液涂敷在NaCl晶片上,红外灯下干燥成膜,用日本IR-435型IR测定。
(2)包埋率的测定
采用溶剂萃取法来测定微胶囊中芯材的含量,即微胶囊的包埋率。包埋率定义如下:包埋率=(抽提后烧瓶重-空烧瓶重)/抽提前试样的重量×100%:
选用乙醇作溶剂,计算公式见下式,具体测定方法如下:
固体微胶囊→140℃烘干30 min→准确称取M1克破壁→加入溶剂萃取芯材→囊壁在60℃下烘干至恒重→准确称量囊壁质量M2克。
包埋率/%=[ ( M1- M2)/M1]×100%
(3)微胶囊产品的热分析
用热分析表征微胶囊成品包埋率和留香时间的关系。
(4)微胶囊缓释性测试
采用恒温热失重的方法测定聚氨酯香精微胶囊的缓释性能,具体测定方法是:准确称量并记录一定量的干燥微胶囊,将其在70℃烘30 min,准确称量并记录结果,然后再将其在70℃烘30 min,准确称量并记录,这样反复到微胶囊恒重为止。
(5)微胶囊保香能力的测定
经干燥过的香料微胶囊平均分成四份,置于阴凉的通风干燥处备测,每隔三天后取一份,用95%乙醇在索式抽提器上水浴抽提3 h,抽提出的香精乙醇溶液定容于250 mL容量瓶中,用95%乙醇稀释至刻度。用751-GW型紫外分光光度仪测出各自的吸光度,然后在香料浓度-吸光度标准曲线上确定浓度,编制出测试时间和香料残留浓度关系曲线。
3 结果与讨论
3.1 乳化剂用量的影响
表1 乳化剂用量对乳化情况的影响
|
序号 |
香精用量mL |
乳化剂用量mL |
搅拌速度r/min |
乳化时间/h |
实验现象 |
|
1 |
5 |
0.5 |
3000 |
1 |
仍有有未乳化香精 |
|
2 |
5 |
0.8 |
3000 |
1 |
乳化液滴不均匀,但颗粒有所减少 |
|
3 |
5 |
1 |
3000 |
1 |
乳化完全且颗粒均匀 |
|
4 |
5 |
3 |
3000 |
1 |
乳化液滴不均匀但颗粒有所减小 |
|
5 |
5 |
5 |
3000 |
1 |
大部分乳化但不均匀 |
本实验形成的是o/w乳状液,要求乳化剂的HLB值在8~18,而Tween一80是HLB值为15的非离子型乳化剂,符合实验要求,进行乳化剂用量的研究,确定不同用量的乳化剂的使用对乳化效果的影响,如表1所示。
由表l可以看出乳化剂为Tween一80时,香精用量为5 mL,乳化剂用量为l mL即香精和乳化剂用量的体积比为5:l时乳化情况最好。其中水含量对乳化效果及乳化剂用量有部分影响,本实验取去离子水100nL。通过多次试验,确定最佳香精和乳化剂用量的体积比为5:1。
3.2 搅拌速度对乳化状况的影响
搅拌速度对乳化状况的影响非常大,实验研究了不同的搅拌速度对乳化体系的影响,见表2。
表2不同乳化搅拌速度及乳化时间下的乳化状况
|
搅拌速度/(r/min) |
1000~2000 |
3000~4000 |
5000 |
|
乳化时间/min |
80 |
60 |
50 |
|
乳化效果 |
乳化液滴较大 大小分布不很均匀 |
乳化液滴小. 大小分布较均匀 |
乳化液滴十分小 大小分布均匀 |
乳化效果在乳化剂足量的情况下,乳化均质速度在约3000 r/min,经过长时间后,也会接近高速下的乳化效果。随着时间的增长,乳化效果并不会以线性形式增强,变化到一定程度趋向平缓。经过比较,我们采用的乳化均质速度约3000~4000 r/min,乳化时间一般为1 h。
3.3 微胶囊红外光谱的测定
通过对香精及微胶囊的红外图谱分析,来确定聚氨酯是否包结上茉莉香精。微胶囊(MC)本身的特征吸收频率覆盖较广,对于一般有机小分子,在
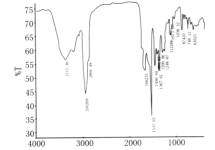
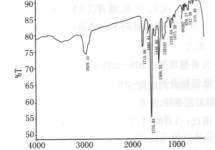
包结物中所占的分量不超过25%(w/w),它们的特征峰容易被Mc的吸收峰掩盖,难以辨认。如果客体分子含有-COOH,-COOR和C=0等基团在1600 cm-1附近有拉伸振动吸收,从峰形、峰位和强度的变化还是能够提供关于客体分子是否进入空腔以及相互作用力性质的证据。茉莉香精的组分主要为酯、醇、烯、酮、酚、醛和烷烃七类化合物。挥发性和半挥发性组分中酯类化合物为主要成分,是香料的原料来源,含-OH、-COOR和C=0等基团,其红外光谱中在1537.93 cm-l处存在强伸缩振动吸收,见图l。包结络合后的香精微胶囊的红外光谱中可看到,在1535.83 cm-l处出现了伸缩振动吸收,见图2所示。说明聚氨酯已包裹了茉莉香精。
|
|
|
|
图1茉莉香精的红外图谱 |
图2茉莉香精微胶囊的红外图谱 |
3.4 包埋率对微胶囊留香期的影响
包埋率和皮芯比用来表征微胶囊对香精的包结情况。下表3为香精微胶囊包埋率及100℃下焙烘测得的留香期。在聚氨酯包结过程中,在一定程度内香精的浓度越大越好,即可置换极性分子的可能性越大,但是香精的浓度并不是唯一影响结合常数的因素,并且内腔的体积很小,对于包结平衡,由于微胶囊内腔体积所限,较高浓度的芯量也不一定达到较好的包结结果,表3所得的包埋率为以下实验提供了数据。
表3 MC的包埋率及100℃焙烘测得留香期
|
编号 |
胶囊原重/g |
壁囊重量/g |
包埋率/% |
留香期/h |
|
l# |
0.7694 |
0.3923 |
49.0l |
5~8 |
|
2# |
0.5330 |
0.2322 |
56.44 |
>13 |
|
3# |
0.5102 |
O.1363 |
73.28 |
<3 |
微胶囊的皮芯比指的是皮材的质量与被包容物质量的比值。在香精微胶囊化过程中,皮材的用量比直接影响了微胶囊的包埋率。本文分别合成了三种不同壁材质量分数的胶囊,在相同的工艺条件下,皮芯比过小,发现聚合结束后,反应体系表面浮有一层油滴,表明存在有未被包覆的芯材,产品经测试,包埋率较高,但经100℃焙烘3 h后,香味消失,说明包埋不彻底,如表3-3#所示。当w(壁材)%=21%时,包埋率较高,留香时间也较长,在100℃焙烘13 h后,仍有明显香味,结果见表3中2#,故本实验中皮芯比1:2~l:3.5为优。
3.5 香精微胶囊的缓释性能的分析
聚合物在包裹芯材的时候会有少量的空洞,这样皮材虽然阻碍了芯材的释放,但由于孔洞的原因使得芯材可以缓慢地释放,这样就形成了缓释型微胶囊。活性物质通过高分子膜向环境中释放,其释放速度取决于颗粒的大小、组成、扩散物质的性质和环境条件,随着这些条件的固定,其释放速度也就固定了。采用恒温热失重的方法测定聚氨酯香精微胶囊的缓释性能。通过这个方法,测得以下恒温热失重实验数据,见图3。
因为胶囊的芯材是通过渗透的方法向外释放的,因此,温度增高可以加剧芯材分子的活动,使得芯材释放更迅速。为了快速描述微胶囊释放规律,我们采用了程序升温的热分析方法和保持高温恒温测定胶囊热失重的方法强迫芯材的释放以便测定胶囊的缓释性。
|
|
|
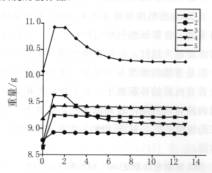
图3热失重法测微胶囊缓释性能比较图 |
由图3可知,70℃下样品在开始的情况下有一段快速的释放,那可能是由于微胶囊吸收的一些水分,以及少量未被包裹的香精而产生的,而以后始终保持着较为平缓的释放量。由图3可直观地看到微胶囊样品的缓释性能,缓释性由好到坏顺序为:
2#>4#>l#>3#>5#,
由表3知这些样品的包埋率,其中l#包埋率为49.01%,2#包埋率为56.44%,5#包埋率为73.28%。对比可知,2#样品的包埋率较高,且其缓释性也较好,为较理想的香精微胶囊样品,与前面测得的包埋率对微胶囊留香期影响的结果一致。
3.6 微胶囊紫外光谱图的分析
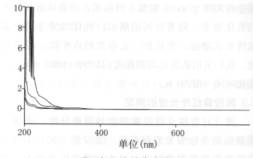
微胶囊紫外光谱图的分析采用的是2#微胶囊样品。用紫外测微胶囊保香的原理:把香料配成不同浓度的标准染液,用紫外测出吸光度,绘制香料的吸光度与浓度的标准曲线图。用紫外测出抽提香料的吸光度,根据其吸光度值在香料的吸光度与浓度的标准曲线上找出相应的浓度值,从而知道香料的变化情况。图4~6分别是茉莉香料紫外图谱、抽提香料紫外图谱和茉莉香料标准曲线图。
|
|
|
|
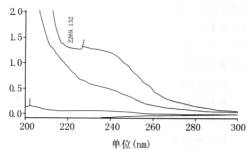
图4茉莉香料和抽提香料紫外图谱 |
图5抽提香料紫外图谱 |
|
|
|
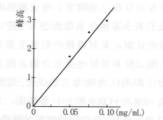
图6茉莉香料标准曲线图 |
图5是0.025 mg/mL,0.05 mg/mL,0.075 mg/mL,0.1 mg/mL浓度下绘制的茉莉香料吸光度与浓度的标准曲线图。
在图5中虽然不能很清楚地看出抽提香料的吸光度值,但从大概的吸光度值在图6中找出对应的浓度值也可以看出微胶囊中香料的变化。虽然第一份抽提香料由于稀释不够,导致浓度过高,无法看清其吸光度值,但其余三份抽提香料的吸光度值变化不大,而吸光度与浓度成正比关系,故相应的浓度变化不大,缓释性好,保香能力强。
3.7 芳香整理
将毛巾在110℃下烘干,使纤维素分子内吸附的水分子脱去。然后用香料微胶囊进行芳香整理:
(1)工艺流程:
织物→浸轧(轧液率70%~80%)→烘干(50~90℃)或自然阴干→成品。
(2)配方:
芳香整理剂:20%~25%扩散剂:0.5g/L~1g/L 低温粘合剂:0~3%
(3)工艺条件:
浴比:1:10~1:20 温度:40℃ 时间:20 min~30 min
表4 洗涤后留香效果
|
洗涤次数 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
放置天数(天) |
2 |
2 |
2 |
2 |
1 |
1 |
1 |
2 |
1 |
1 |
|
留香程度(干后) |
+++ |
+++ |
+++ |
++ |
++ |
++ |
++ |
++ |
+ |
+ |
如表4所示,将整理的织物在半月内洗涤10次,每次洗涤后晾干,进行嗅觉判断,直到第10k洗涤后晾干后仍残留有淡淡的香味。
4结论
l、氨酯芳香微胶囊的最佳实验工艺:
(1)最佳的皮芯比选取1:2~1:3.5,制备预聚物时异氰酸酯与PEG的摩尔比应为3:1,PEG/丙酮浓度=0.03mol/L:
(2)选用Tween-80-~L化剂,乳化剂与香精的用量比为1:5,乳化剂/水体积比=l:10:
(3)在3000~4000r/min乳化均质速度下,乳化时间一般为lh:
(4)包结的温度不宜太高,一般为60℃,扩链剂(邻苯二酚)/TDI的摩尔比:1/4:
2、用红外光谱对微胶囊进行分析,得到香料被成功包裹,用恒温热失重法测定了香精微胶囊缓释性能,应用热分析技术对香精微胶囊的包埋率进行了定量的测定,微胶囊最佳包埋率为56。44%留香期大于13h。
3、将制得的香料微胶囊在毛巾和棉布上进行芳香整理,获得了较理想的效果。
参考文献
[1]武伟.微胶囊的控制释放作用及其在食品工业中的应用[J]食品研究与开发,2001,2:26.
[2]Baumgartner,S.,Kristl,J.,Vrever,F.,et a1.Optimisation of floating matrix tabletS and evaluation of their gastric residence time[J]Int.J.Pham,2000,2:125―135.
[3]Deshpande,A.A.,Rhodes,C.T.,Shah,N.H.,et a1.Controlled―release drug delivery systems for prolonged gastric residence[J].an overview,Drug DeV.Ind.Pham,1996,4:53l-539.
[4]Desponded,A.A.,Shah,N.H.,Rhodes,C.T.,et a1.Development of a novel control led release system for gastric retention[J].Phar~Res.,1997,6:815―819.
[5]Fel 1,J.T.,Del ivery systems for target ing to specific sites in the gastrointestinal tract[J] Phar~Pharmacol,1999,3:41.
[6]He,P.,Davis,S.S.,Illu~L.,Sustained release chitosan microspheres prepared by novel spray drying methods[J].Microencapsulation,1999,3:343―355.
[7]Lin,S.Y.,Lin,P.C.,Effect of acj d type,acetic acid and sodi,m carboxy methyl cellulose concentration on the formulation,micromeritic。dissolution and floating properties of theophyllin chitosan microcapsules[J].Chem.Pharm.Bull,1992,1:2491―2497.
[8]Menon,A,Ritschel,W.A.,Sakr,A.,Development and evaluation of a monolithic floating dosage form for urosemide[J]Phar~Sci.,1994,2:239-245.
[9] Benita Simon,Microencapsulation[M].Newyork:Basel Hongkong,1996.
[10]Nixon J
R,Preparation of microcapsules with possible pharmaceutical use
[J]Endeavour,1985,9;123-128
[11]Kas h.s.,Review:chitosan:properties,preparations and application to microparticulate systems [J] Microencapsulation.1997,3;689-711
[12]Kawshima,Y.,Handa,T.,Kasai,A.,Tal‘enaka,H.,Lin,S.Y.,And0,Y.,Nov method for the preparation of contro11ed-release theophylline granules coated with a po1yelectro1yte complex of sodium polyphosphate―chitosan[J].Pharm Sci,1985,5:264―268.
[13]Szente L,Szejtli J.Flavor Encapsulation[M].New 0rleans,hmericall Chemical Symposium Series370,1987:148―157.