(编者注:本资料摘自《超星数字图书馆》藏书;本文重点摘录药物微胶囊应用与发展、常用囊材与载体材料、工艺制作三个内容。工艺方面祗摘录了;相分离法、单凝聚法、复凝聚法、溶剂-非溶剂法四种,并且其中有些图片因复制不清而省略;标题是编者加的)
常用囊材与载体材料
陆彬;药物新剂型与新技术,1998;168-170
微囊的囊心物与微球的内容物除主药外可以加入附加剂,如稳定剂、稀释剂以及控制释放速率的阻滞剂、促进剂等。通常将主药与附加剂混匀后微囊化,亦可先将主药单独微囊化,再加入附加剂。若有多种主药,可将其混匀再微囊化,亦可分别微囊化后再混合,这取决于药物、材料和附加剂的性质及工艺条件等。下面主要讨论囊材或载体材料。
囊材或载体材料是用于包囊、制作微球或毫微粒所需的材料,一般的要求是:①性质稳定;②有合宜的释药速率;③无毒、无刺激性;④能与药物配伍,不影响药物的药理作用及含量测定;⑤有—定的强度及可塑性、能完全包封囊心物,或药物与附加剂能比较完全地进入球的骨架内;⑥具有符合要求的粘度、渗透性、亲水性、溶解性等特性。
常用的囊材与载体材料可分为天然的、半合成或合成的高分子材料,现简述如下。
(一)天然高分子 天然高分子材料是最常用的囊材与载体材料,因其稳定、无毒、成膜性或成球性较好。
1、明胶 明胶是氨基酸与肽交联形成的直链聚合物,通常是Mav(平均相对分子质量)在15000-25000之间不同M r(相对分子质量)的混合物。因制备时水解方法的不同.明胶分酸法明胶(A型)和碱法明胶(B型)。A型明胶的等电点为7-9,10g/L溶液25℃的pH为3.8-6.0,B型明胶稳定而不易长菌,等电点为4.7-5,10g/L溶液25℃的pH为5-7.4。两者的成囊性或成球性无明显差别,溶液的粘度均在0.2-0.75 cPa·s之间。可生物降解,几乎无抗原性,通常可根据药物对酸碱性的要求选用A型或B型,用作微囊的用量为20-100g/L,用作微球的量可达200g/L以上。
2.阿拉伯胶 一般常与明胶等量配合使用,作囊材的用量为20-100g/L,亦可与白蛋白配合作复合材料。英国产品的等电点为2.4。
3.海藻酸盐 系多糖类化合物,常用稀碱从褐藻中提取而得。海藻酸钠可溶于不同温度的水中,不溶于乙醇、乙醚及其它有机溶剂;不同Mav产品的粘度有差异。可与甲壳素或聚赖氨酸合用作复合材料。因海藻酸钙不溶于水,故海藻酸钠可用CaCl2固化成囊。研究各种灭菌方法对海藻酸盐的影响,发现高温灭菌(120℃、20分钟)使其10g/L溶液的粘度降低64%;低温加热(80℃、30分钟)几个循环对灭菌效果较差,反而促使海藻酸盐逐步断键;用环氧乙烷灭菌也引起粘度降低和断键;膜过滤除菌的产物粘度和Mav都不变。
4. 蛋白类 常用作载体材料的有白蛋白(如人血清白蛋白、小牛血清白蛋白)、玉米蛋白、鸡蛋白、小牛酪蛋白等,可生物降解,无明显的抗原性.常采用加热固化或化学交联剂(如甲醛、戊二醛或丁二烯)固化.通常用量在300g/L以上。
5.淀粉 有玉米淀粉、小麦淀粉、马铃薯淀粉等.其来源不同,分子中直链和支链的结构也不同.不溶于冷水及乙醇。用作囊材或载体材料的常为淀粉的衍生物.如羟乙基淀粉、羧甲基淀粉及马来酸酯化淀粉-丙烯酸共聚物等。
(二)半合成高分子 多系纤维素衍生物,如羧甲基纤维素、邻苯二甲酸醋酸纤维素、甲基纤维素、乙基纤维素、羟丙甲纤维素、丁酸醋酸纤维素、琥珀酸醋酸纤维素等。其特点是毒性小、粘度大、成盐后溶解度增大;由于易水解,故不宜高温处理,需临用时现配。
1.羧甲基纤维素盐(如SCMC) 属阴离子型的高分子电解质.常与明胶配合作复合囊材,一般分别配l-5g/L SCMC及30g/L明胶,再按体积比2︰l混合。SCMC遇水溶胀,体积可增大10倍,在酸性液中不溶。水溶液粘度大,有抗盐能力和一定的热稳定性.不会发酵,也可以制成CMCAl单独作囊材。
2.邻苯二甲酸醋酸纤维素(CAP) 在强酸中不溶解,可溶于pH>6的水溶液.分子中含游离羧基,其相对含量决定其水溶液的pH值及能溶解CAP的溶液的最低pH值。用作囊材时可单独使用,用量一般在30g/L左右,也可与明胶配合使用。
3.乙基纤维素(EC) 乙基纤维素的化学稳定性高,适用于多种药物的微囊化,不溶于水、甘油和丙二醇,可溶于乙醇.遇强酸易水解,故对强酸性药物不适宜。
4.甲基纤维素(MC) 用于微囊作囊材的用量为10-30g/L.亦可与明胶、SCMC、聚乙烯吡咯烷酮(PVP)等配合作复合囊材。
5.羟丙甲纤维素(HPMC) 能溶于冷水成为粘性胶体溶液.长期贮存稳定性高.有表面活性,表面张力(42-56)×10-5N/cm。
(三)合成高分子 合成高分于材料常用的有两类.可生物降解的和不可生物降解的。近年来,可生物降解并可生物吸收的材料受到普遍的重视并得到广泛的应用。
如聚碳酯、聚氨基酸、聚乳酸(PLA)、聚丙烯酸树脂、聚甲基丙烯酸甲酯、聚甲基丙烯酸羟乙酯、聚氰基丙烯酸烷酯、乙交酯丙交酯共聚物、聚乳酸-聚乙二醇嵌段共聚物(PLA-PEG)、ε-己内酯与丙交酯嵌段共聚物、聚合酸酐及羧甲基葡聚糖等。其特点是无毒、成膜及成球性好、化学稳定性高,可用于注射。下面重点介绍几种。
1.聚酯 聚酯类是迄今研究最多、应用最广的可生物降解的合成高分子.它们基本上都是羟基酸或其内酯的聚合物。常用的羟基酸是乳酸(Lactic acid)和羟基乙酸(glycolic acid)。乳酸包括D-型、L-型及DL-型,直接由其中一种缩合得到的聚酯,分别用P(D)LA、P(L)LA和P(DL)LA表示,由羟基乙酸缩合得到的聚酯用PGA表示;由—种乳酸与羟基乙酸直接缩合的,分别用P(D)LAGA、P(L)LAGA和P(DL)LAGA表示。由D-型、L-型、DL-丙交酯通过开环聚合而得的聚酯,分别用P(D)L、P(L)L和P(DL)L表示:由L-丙交酯与DL-丙交酯制得的嵌段共聚物用P(L)L(DL)L表示;由D-型、L-型、DL-丙交酯通过与乙交酯开环聚合而得的聚酯,分别用P(D)LG、P(L)LG和P(DL)LG表示。
聚酯的特性常用热分析法测定,包括差示热分析(DTA)及差示扫描量热法(DSC),测定的主要参数是玻璃化温度Tg和晶体的熔点Tm(当聚合物有一定程度的结晶性时),热分析也可了解载药微囊(球)的结构及其变化。表5-1列出一些可生物降解的聚酯的Mav、Tg及Tm,其中仅P(DL)L测不出结晶度。表中未写出Mav的,所给出的Tg、Tm为Mav约为40000的产品的常数(Mav再高.这些常数基本不变)。
表5-1 一些可生物降解的聚酯的特性常数
|
聚酯 |
Mav |
Tg(℃) |
Tm(℃) |
|
P(DL)L |
- 20,500 13,300 5,200 |
57 54.5 53.5 50.5 |
- - - - |
|
P(D)L |
- - |
67 67 |
180 173 |
|
P(L)LA |
8,800 2,400 |
44 58 |
142 173 |
|
P(98L/2D)LA* |
4,690 |
40 |
134 |
|
P(92D/8L)LA |
4,650 |
34 |
115 |
|
PGA |
- |
36 |
230 |
|
PCLb |
- |
65 |
63 |
|
PHB |
- |
- |
175-177 |
注; *括弧内数字表示摩尔比;b聚已内酰胺
这些聚合物都表现出一定的融蚀降解的特性,结晶度低的降解较快、聚乳酸[P(DL)LA]的Mav范围在1万-40万,降解周期为2-12个月,Mav=90,000的熔点为60℃,在体内6个月降解。有人用聚3-羟基丁酸酯(PHB)为囊材制成胰岛素微囊注射剂,在体内3个月降解。又如消旋丙交酯-乙交酯共聚物[P(DL)LG],在共聚时有各种比例,若丙交酯︰乙交酯=75︰25的共聚物为囊材,在体内1个月可降解,如85︰15的为囊材,在体内3个月降解。PEG被美国FDA批准为无毒、可供内服的辅料,促进其在制剂中的进一步应用。PEG可与药物分子或毫微球结合而减小被内皮系统吞噬的可能,明显提高药物在循环系统中存在的时间,尤其是应用于提高蛋白质类的循环半衰期。。PLA-PEG嵌段共聚物(P(DL)LA-PEG)中D,L-PLA为疏水性,PEG为亲水性,调节二者的比例及共聚物的Mr可控制其降解性能,体外降解周期可控制在1-9个月范围内,从而控制微粒中药物的释放速率。
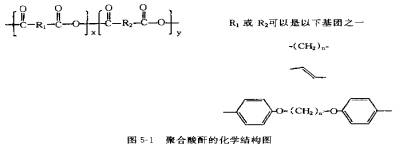
2.聚合物酸酐 聚合酸酐的基本结构是[CO-R1-COO]x [CO-R2-COO]y,其中Rl、R2的单体有链状,也有环状的,化学结构见图5-l。
聚合酸酐的Mav常在2,000-200,000之间,可由凝胶透过色谱法(GPC)测定,用聚苯乙烯Mav标准校正。其特征峰可用红外测定。
应用高分子附加剂并调整其它参数,可控制微粒的粘连和聚集。为了控制注射用微粒的质量,达到有关生物相容性的要求,已对人工合成的、多为疏水性的高分子材料作了更为深入的研究。